化学学习中,推理是一种重要的学习方法,下列推论正确的是( )
| A.由“BF3和SO3互为等电子体”,可推知二者均为非极性分子 |
| B.由“某过程发生化学键断裂”,可推知该过程发生了化学变化 |
| C.由“蒸干NaCl溶液得NaCl固体”,可推知蒸干MgCl2溶液得MgCl2固体 |
| D.由“同温度下等浓度的Na2CO3溶液比Na2SO3溶液的pH大”,可推知C比S的非金属性弱 |
20世纪80年代后,人们发现并证实了碳的另一类单质,它们是由一系列偶数个碳原子构成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关物质X的说法不正确的是( )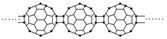
| A.X难溶于水 |
| B.一定条件下X可与H2发生加成反应 |
| C.X的摩尔质量为720n |
| D.X是碳的一种同素异形体 |
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是( )
| A.XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY |
| B.XYZ3是一种微溶于水的盐,且Y与Z可形成共价化合物化合物YZ或YZ2 |
| C.XYZ3是一种易溶于水的盐,且X与Z可形成离子化合物XZ |
| D.XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3 |
以下物质的分子可用比例模型 表示的是
表示的是
| A.CO2 | B.H2O | C.N2O | D.HClO |
硼及其化合物在催化剂制造、储氢材料、燃料电池等方面应用广泛。Li3BN2是一种价格低廉且性能优良的储氢材料,其储氢与放氢原理为Li3BN2+4H2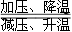 Li3BN2H8。下列有关说法正确的是
Li3BN2H8。下列有关说法正确的是
| A.B的原子半径小于N的原子半径 |
| B.H2的结构式为H—H |
| C.放氢过程为化合反应 |
| D.储氢过程没有能量变化 |
下列物质既含离子键又含共价键的是
| A.CO2 | B.NaOH | C.CaCl2 | D.C6H6 |
下列物质中,含有共价键的是
| A.MgCl2 | B.CH4 | C.Na2O | D.KBr |
砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是
| A.分子中共价键键角均为109°28′ | B.黄砷中共价键键能大于白磷 |
| C.黄砷分子极性大于白磷 | D.黄砷的熔点高于白磷 |
下列变化需克服共价键的是
| A.金刚石熔化 | B.汞受热变成汞蒸气 | C.蔗糖溶于水 | D.食盐溶于水 |
下列说法正确的是
| A.NH4Cl为共价化合物 |
| B.N2分子中含有一对共用电子对 |
| C.Na2O2既含有离子键又含有非极性键 |
| D.电解水与电解熔融NaCl时破坏的化学键类型相同 |