题目内容
下列说法正确的是
| A.NH4Cl为共价化合物 |
| B.N2分子中含有一对共用电子对 |
| C.Na2O2既含有离子键又含有非极性键 |
| D.电解水与电解熔融NaCl时破坏的化学键类型相同 |
C
解析试题分析:A、NH4Cl为离子化合物,故A错误;B、N2分子中含有三对共用电子对,故B错误;C、Na2O2既含有离子键又含有非极性键正确;D、电解水破坏的是共价键,电解熔融NaCl破坏的是离子键,故D错误。
考点:化学键与晶体结构

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一种新催化剂,能在室温下催化空气氧化甲醛:HCHO+O2 CO2+H2O,该反应
CO2+H2O,该反应
| A.反应物和生成物中都含极性分子和非极性分子 |
| B.生成1.8gH2O消耗2.24L O2 |
| C.反应时有极性键和非极性键的断裂和它们的生成 |
| D.为吸热反应 |
硼及其化合物在催化剂制造、储氢材料、燃料电池等方面应用广泛。Li3BN2是一种价格低廉且性能优良的储氢材料,其储氢与放氢原理为Li3BN2+4H2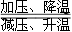 Li3BN2H8。下列有关说法正确的是
Li3BN2H8。下列有关说法正确的是
| A.B的原子半径小于N的原子半径 |
| B.H2的结构式为H—H |
| C.放氢过程为化合反应 |
| D.储氢过程没有能量变化 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CCl4和KCl | C.NaCl和HCl | D.CO2和H2O |
对σ键和π键的认识不正确的是
| A.σ键和π键不属于共价键,是另一种化学键 |
| B.s-sσ键与s-pσ键的电子云均为轴对称图形 |
| C.分子中含有共价键,则至少含有一个σ键 |
| D.含有π键的化合物与只含σ键的化合物的化学性质不同 |
下列各元素的原子在形成不同物质时,既能形成非极性键,也能形成极性键,还能形成离子键的是( )。
| A.Na | B.Fe | C.O | D.Ar |
PH3是一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断中错误的是( )
| A.PH3分子呈三角锥形 |
| B.PH3分子是极性分子 |
| C.PH3沸点低于NH3沸点,因为P—H键键能低 |
| D.PH3分子稳定性低于NH3分子,因为N—H键键能高 |
下列变化需克服相同类型作用力的是( )
| A.碘和干冰的升华 | B.硅和C60的熔化 |
| C.氯化氢和氯化钠的溶解 | D.溴和汞的气化 |