下列物质的变化过程中,只需克服分子间作用力的是( )
| A.食盐溶解 | B.氯化氢溶于水 | C.干冰升华 | D.氯化铵分解 |
下列现象与氢键无关的是
| A.小分子的醛、羧酸可以与水互溶 |
| B.冰的密度比液态水的密度小 |
| C.邻羟基苯甲酸的溶沸点比对羟基苯甲酸的溶沸点低 |
| D.乙醚与苯混溶 |
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子。下列关于天然气水合物中两种分子极性的描述正确的是 。
| A.两种都是极性分子 |
| B.两种都是非极性分子 |
| C.CH4是极性分子,H2O是非极性分子 |
| D.H2O是极性分子,CH4是非极性分子 |
下列说法正确的是 ( )
| A.H2O的熔点、沸点大于H2S的是由于H2O分子之间存在氢键。 |
| B.HF、HCl、HBr、HI的熔点沸点依次升高。 |
| C.乙醇分子与水分子之间只存在范德华力。 |
| D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH3-),在这个过程中,下列描述不合理的是( )
| A.碳原子的杂化类型发生了改变 |
| B.微粒的形状发生了改变 |
| C.微粒的稳定性发生了改变 |
| D.微粒中的键角发生了改变 |
下列有关叙述中,错误的是( )
| A.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| B.白磷分子晶体中,微粒之间通过共价键结合 |
| C.σ键可以单独存在,π键不可单独存在 |
| D.H2O的分解温度及沸点都比H2S高得多的事实不可都用氢键知识解释 |
下列说法正确的是( )
| A.若把H2S分子写成H3S分子,违背了共价键的饱和性 |
| B.晶体中若有阳离子一定有阴离子 |
| C.金属键存在于任何含金属元素的物质中 |
| D.晶体中一定存在化学键 |
下列分子中的中心原子杂化轨道的类型相同的是( )
| A.CO2与H2O | B.CH4与NH3 | C.BeCl2与BF3 | D.C2H2与C2H4 |
在化学上,常用一条短线表示一个化学键,如下图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是( )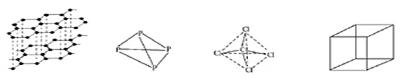
| A.石墨的结构 | B.白磷的结构 | C.CCl4的结构 | D.立方烷(C8H8)的结构 |
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示。以下有关该物质的说法中正确的是( )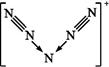
| A.每个N5+中含有35个质子和36个电子 |
| B.该离子中有非极性键和配位键 |
| C.该离子中含有2个π键 |
| D.与PCl4+互为等电子体 |