下列用电子式表示的形成过程正确的是( )
A.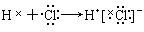 |
B.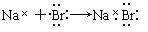 |
C.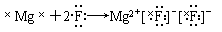 |
D. |
下列物质中,既有离子键,又有非极性共价键的是
| A.H2O | B.CaCl2 | C.KOH | D.Na2O2 |
下列电子式中,正确的是
A. | B. | C. | D. |
有关物质结构的叙述中,正确的是
| A.只含有共价键的物质不一定是共价化合物 |
| B.由电子定向移动而导电的物质一定是金属晶体 |
| C.有键能很大的共价键存在的物质熔沸点一定很高 |
| D.原子晶体中只存在非极性共价键 |
北大和中科院已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。有关分析正确的是
| A.K3C60中只有离子键 | B.K3C60中碳元素显-3价 |
| C.该晶体在熔融状态下能导电 | D.该晶体熔点较低 |
下列物质中不存在氢键的是
| A.水 | B.甲醇 | C.乙醇 | D.乙烷 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| C.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |
σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成。则下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的是( )
| A.H2 | B.HCl | C.Cl2 | D.F2 |
下列关于丙烯(CH3—CH =CH2)的说法正确的
| A.丙烯分子有7个δ键,1个∏键 |
| B.丙烯分子存在非极性键 |
| C.丙烯分子中3个碳原子都是sp3杂化 |
| D.丙烯分子中3个碳原子在同一直线上 |
实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°。由此可见,BeCl2属于( )
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.由非极性键构成的非极性分子 |