下列说法正确的是
| A.构成单质分子的微粒一定含有共价键 |
| B.熔融时能导电的化合物,一定是离子化合物 |
| C.水加热至1000℃也不分解,是由于水分子间存在氢键 |
| D.由H原子形成1molH-H键所要吸收的能量就等于H-H的键能 |
氮化硼是一种新合成的结构材料,具有超硬、耐磨、耐高温的特点。下列各组物质熔化时,所克服的微粒间作用力与氮化硼熔化所克服的微粒间作用力都不相同的是
| A.氯化钠和金刚石 | B.晶体硅和二氧化硅 |
| C.冰和干冰 | D.二氧化硫和二氧化硅 |
下列图像表达正确的是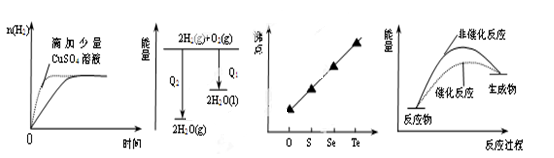
| A.等质量锌粉与足量盐酸反应 |
| B.氢气与氧气反应中的能量变化 |
| C.气态氢化物沸点 |
| D.催化反应与非催化反应过程中的能量关系 |
下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C—O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
下列过程中化学键被破坏的是
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水⑤MgCl2溶解于水 ⑥NaCl熔化
| A.全部 | B.②③④⑤⑥ | C.④⑤⑥ | D.⑤⑥ |
关于化学式[TiCl(H2O)5]Cl2·H2O的配合物的下列说法中正确的是
| A.配位体是Cl-和H2O,配位数是9 |
| B.中心离子是Ti4+,配离子是[TiCl(H2O)5]2+ |
| C.内界和外界中的Cl-的数目比是1:2 |
| D.加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108.1°,下列有关N(NO2)3的说法正确的是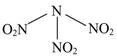
| A.分子中N、O间形成的共价键是非极性键 | B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 | D.15.2 g该物质含有6.02×1022个原子 |
下列描述中正确的是
| A.CS2为V形的极性分子 | B.ClO3-的空间构型为平面三角形 |
| C.SF6中的空间构型为正四面体形 | D.SiF4和SO32-的中心原子均为sp3杂化 |
下列各项比较中前者高于(或大于或强于)后者的是
| A.CCl4和SiCl4的熔点 |
B.邻羟基苯甲醛(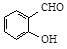 )和对羟基苯甲醛( )和对羟基苯甲醛(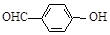 )的沸点 )的沸点 |
| C.SO2和CO2在水中的溶解度 |
| D.H2SO3和H2SO4的酸性 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CCl4和KCl | C.NaCl和HCl | D.CO2和H2O |