电子数相等的微粒叫做等电子体,下列各组微粒属于等电子体是
| A.CO和CO2 | B.NO和CO | C.CH4和NH3 | D.OH- 和S2- |
下列叙述正确的是
| A.非金属原子间以共价键结合的物质一定是共价化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.凡是能电离出离子的化合物一定是离子化合物 |
| D.凡是含有离子键的化合物一定是离子化合物 |
关于晶体的下列说法正确的是( )
| A.化学键都具有饱和性和方向性 |
| B.晶体中只要有阴离子,就一定有阳离子 |
| C.氢键具有方向性和饱和性,也属于一种化学键 |
| D.金属键由于无法描述其键长、键角,故不属于化学键 |
下列推断正确的是 ( )
| A.BF3是三角锥形分子 |
B.NH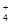 的电子式: 的电子式: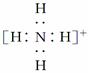 ,离子呈平面形结构 ,离子呈平面形结构 |
| C.CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的p轨道形成的sp σ键 |
| D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个s-sp3 σ键 |
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,以下判断正确的是( )
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.BeCl2中Be采取sp2杂化 |
下列有关叙述正确的是
| A.氢键是一种特殊化学键,它广泛地存在于自然界中 |
| B.在CH3—CHOH—COOH分子中含有1个手性C原子 |
| C.碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D.含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
下列各组微粒属于等电子体的是( )
| A.CO和CO2 | B.NO和NO2 | C.CH4和NH3 | D.CO2和N2O |
[Co(NH3)5Cl]2+配离子,中心离子的配位数是( )
| A.1 | B.2 | C.4 | D.6 |
下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH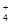 和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO
和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO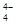 和SO
和SO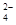
| A.全部 | B.除①④⑥以外 | C.③④⑤⑥ | D.②⑤⑥ |
下列说法正确的是( )
| A.离子晶体中可能含有共价键,一定含有金属元素 |
| B.分子晶体中可能不含共价键 |
| C.非极性分子中一定存在非极性键 |
| D.对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |