题目内容
下列各组微粒属于等电子体的是( )
| A.CO和CO2 | B.NO和NO2 | C.CH4和NH3 | D.CO2和N2O |
D
解析试题分析:原子数和价电子数分别都相等的微粒为等电子体,分子中质子数等于电子数,则A、CO和CO2的原子数和价电子数分别均不相等,所以两者不是等电子体,故A错误;B、NO和NO2的原子数和价电子数分别均不相等,所以两者不是等电子体,故B错误;C.CH4和NH3的原子数不相等,不属于等电子体,故C不正确;D、CO2和N2O的原子数和价电子数分别均相等,所以两者是等电子体,故D正确,答案选D。
考点:考查等电子体判断

练习册系列答案
相关题目
已知BeCl2为共价化合物。 下列对于BeCl2分子的说法正确的是
| A.由极性键构成的极性分子 | B.由非极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.由极性键构成的非极性分子 |
下列电子式书写正确的是
A.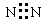 | B. | C.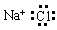 | D.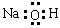 |
下列关于丙烯(CH3—CH=CH2)的说法正确的是
| A.一个丙烯分子中有8个σ键和1个π键 |
| B.丙烯分子中3个碳原子可能在同一直线上 |
| C.丙烯分子中3个碳原子都是sp3杂化 |
| D.丙烯分子中不存在非极性键 |
下列说法正确的是( )
| A.CHCl3是正四面体形 |
| B.H2O分子中氧原子为sp2杂化,其分子几何构型为V形 |
| C.二氧化碳中碳原子为sp杂化,为直线形分子 |
D.NH 是三角锥形 是三角锥形 |
下列叙述正确的是
| A.非金属原子间以共价键结合的物质一定是共价化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.凡是能电离出离子的化合物一定是离子化合物 |
| D.凡是含有离子键的化合物一定是离子化合物 |
下列物质中既含有共价键又含有离子键的是
| A.HF | B.NaCl | C.HCl | D.K2SO4 |
某元素的原子最外层只有一个电子,它跟卤族元素结合时形成的化学键
| A.一定是共价键 | B.一定是离子键 |
| C.可能是共价键,也可能是离子键 | D.上述说法都不正确 |
下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是
| A.液溴和苯分别受热变为气体 | B.干冰和氯化铵分别受热变为气体 |
| C.二氧化硅和铁分别受热熔化 | D.食盐和葡萄糖分别溶解在水中 |