已知W.X.Y.Z为短周期元素,W.Z同主族,X.Y.Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X.Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.W与X形成的化合物中只含离子键 |
| B.X、Y、Z、W的原子半径依次减小 |
| C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
短周期金属元素甲-戊在元素周期表中的相对位置如表所示,下面判断正确的是( )
| 甲 | 丙 | |
| 乙 | 丁 | 戊 |
A.原子半径: 丙<丁<戊
B.金属性:丙>甲
C.最高价氧化物对应的水化物碱性:乙>丁>戊
D.戊只与强酸反应
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
| | X | | |
| Y | Z | | W |
A.原子半径:rW>rZ>rY>rX
B.含Y元素的盐溶液有的显酸性,有的显碱性
C.最简单气态氢化物的热稳定性:Z>W
D.X与氢元素组成的化合物XH5与水反应可产生两种气体
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如图所示变化。己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。下面判断正确的是
| A.原子半径:Z<Y<X | B.非金属性:Z>Y>X |
| C.化合物A易溶于水 | D.化合物B与C的混合物呈碱性 |
下列叙述与对应图式正确的是
A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强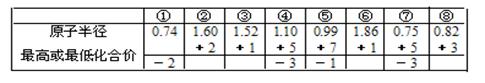 |
B.图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2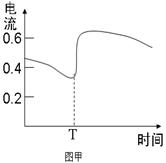  |
| C.图乙表示某一放热反应,若使用催化剂E1、E2、ΔH都会发生改变 |
| D.表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ/mol |
甲、乙、丙、丁四种短周期主族元素,它们的价电子数依次增大,乙形成的化合物种类最多,甲与乙的原子序数之和等于丁的原子序数,丙和乙位于同一周期,丁和乙位于不同周期。则下列说法中正确的是
| A.甲、乙、丙形成的化合物既有离子键又有共价键 |
| B.乙、丙、丁形成的氢化物常温下均为气体 |
| C.原子序数由小到大顺序为:甲<乙<丙<丁 |
| D.原子半径大小顺序为:丁>甲>乙>丙 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价。下列说法正确的是
| A.XH4的沸点比YH3高 |
| B.X与W形成的化合物和Z与W形成的化合物的化学键类型相同 |
| C.元素W的最高价氧化物对应水化物的酸性比Y的强 |
| D.X与Y形成的化合物的熔点可能比金刚石高 |
短周期元素X、Y、Z中,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1个,下列比较正确的是
| A.原子半径:X>Y | B.元素非金属性:X>Y |
| C.气态氢化物的稳定性:Z>Y | D.最高价氧化物水化物的酸性:Z>Y |
