3He可以作为核聚变材料。下列关于3He的叙述正确的是
| A.3He和3H互为同位素 | B.3He原子核内质子数为3 |
| C.3He原子核内中子数为1 | D.3He原子易失去两个电子 |
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是( )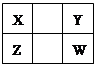
| A.Z元素的原子半径可能比Y元素的小 |
| B.Z的原子序数不可能是X的原子序数的2倍 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的最高价氧化物的水化物的酸性一定比W的强 |
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是
| A.X2-的还原性一定大于Y- |
| B.由mXa+与nYb-得m+a=n-b |
| C.X、Y一定不是同周期元素 |
| D.若X的原子半径大于Y,则气态氢化物的稳定性一定是X大于Y |
下列各项内容中,排列顺序正确的是
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3 ②物质的熔点Li>Na>K
③微粒半径:K+>S2->F- ④单质的密度Na<K<Rb ⑤氢化物的沸点:H2Se>H2S>H2O
| A.①③ | B.②④ | C.①② | D.③⑤ |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2 |
若元素X位于ⅠA族,Y为短周期元素,X与Y可形成化合物X2Y,下列说法正确的是( )
| A.X的原子半径一定大于Y的原子半径 |
| B.X与Y的简单离子不可能具有相同的电子层结构 |
| C.两元素形成的化合物中,原子个数比不可能为1:1 |
| D.X2Y可能是离子化合物,也可能是共价化合物 |
砷是第4周期第ⅤA族非金属元素,下列关于砷的推测不正确的是( )
| A.属于短周期元素 | B.可以存在-3、+3、+5等多种化合价 |
| C.砷在通常情况下是固体 | D.最高价氧化物As2O5属于酸性氧化物 |
下列递变规律正确的是( )
| A.Na、Mg、Al的金属性依次减弱 |
| B.P、S、Cl元素的最高正价依次降低 |
C.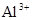 、 、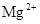 、 、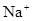 的离子半径依次减小 的离子半径依次减小 |
| D.HNO3、H3PO4、H2SO4酸性依次增强 |
随着卤素原子半径的增加,下列递变规律正确的是( )
| A.单质的熔沸点逐渐降低 | B.卤素离子的还原性逐渐增强 |
| C.最高正化合价逐渐增大 | D.单质的氧化性逐渐增强 |
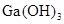 是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。
是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________和________。