已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是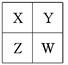
| A.W的原子序数可能是Y的原子序数的2倍 |
| B.Z元素的原子半径可能比Y元素的小 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的化学活泼性一定比X强 |
下列各选项所述的两个量,前者一定大于后者的是
①3d轨道的能量和4s轨道的能量;②同一电子层中第一个p轨道与第二个p轨道的能量;③2s和3s的轨道半径;④同一原子的基态和激发态;⑤F元素和O元素的电负性;⑥Mg元素和Al元素的第一电离能;⑦H原子和H+离子的半径
| A.①⑤⑥⑦ | B.②③⑤ | C.②④⑦ | D.全对 |
若某一个原子在处于能量最低状态时,外围电子排布为4d15s2,则下列各项说法正确的是
| A.该元素原子最外层共有3个电子 |
| B.该元素位于第5周期ⅡA族 |
| C.该元素原子核外第N层上共有9个不同状态的电子 |
| D.该元素原子第四电子层上有5个空轨道 |
在2p能级上最多只能排布6个电子,其依据的规律是
| A.能量最低原理 | B.泡利不相容原理 |
| C.洪特规则 | D.能量最低原理和泡利不相容原理 |
下列选项的说法中正确的是
| A.1s22s12p1表示的是激发态原子的电子排布 |
| B.3p2表示3p能级有两个原子轨道 |
| C.同一原子中,1s、2s、3s电子的能量逐渐减小 |
| D.同一原子中,2p、3p、4p能级的轨道数依次增多 |
现有四种元素的基态原子的电子排布式如下 ①1s22s22p63s23p4 ②1s22s22p63s23p3; ③1s22s22p5下列正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.不成对电子数:③>②>① |
4p轨道电子排布达到半充满的元素,其原子序数是
| A.15 | B.33 | C.35 | D.51 |
气态中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是
| A.1s22s22p63s23p2→1s22s22p63s23p1 |
| B.1s22s22p63s23p3→1s22s22p63s23p2 |
| C.1s22s22p63s23p4→1s22s22p63s23p3 |
| D.1s22s22p63s23p63d104s24p1 →1s22s22p63s23p63d104s2 |
基态原子的价电子构型3s23p3,下列关于它的描述正确的是
| A.该元素的电负性小于1.8 |
| B.3p能级上的3个电子能量相等,自旋状态相同 |
| C.它的氢化物分子中有四个键合电子 |
| D.该元素的价电子数是4 |