元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是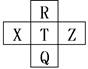
| A.非金属性:T<X <R |
| B.气态氢化物稳定性:R <T<Q |
| C.R与Q的电子数相差16 |
| D.X与Q最高价氧化物的水化物的质子数相差18 |
硫化氢分子中,形成共价键的原子轨道是
| A.硫原子的2p轨道和氢原子的1s轨道 |
| B.硫原子的2p轨道和氢原子的2p轨道 |
| C.硫原子的3p轨道和氢原子的1s轨道 |
| D.硫原子的2p轨道和氢原子的3p轨道 |
X、Y、Z、W、R、E是六种短周期元素,右图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是
| A.原子半径:Z>W>R>E |
| B.R的气态氢化物比X的气态氢化物沸点高 |
| C.Z与Y可形成既含离子键又含共价键的化合物 |
| D.Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物能发生反应 |
已知第三周期元素M,其原子最外层达到饱和时所需的电子数小于次外层与最内层电子数之差,且等于最内层电子数的正整数倍。下列关于元素M的说法一定错误的是
| A.M元素存在同素异形体 |
| B.M元素为非金属元素 |
| C.M的最高价氧化物对应的水化物都是强酸 |
| D.常温下,能稳定存在的M的氧化物都是酸性氧化物 |
下列说法错误的是
| A.同主族元素的简单阴离子还原性越强,水解程度越大 |
| B.Na和Cs属于IA族元素,Cs失电子的能力比Na强 |
| C.IA族与VIIA族元素间可形成共价化合物或离子化合物 |
| D.同周期元素(0族元素除外)从左到右,原子半径逐渐减小 |
右表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是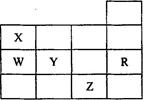
| A.常温常压下,五种元素的单质中有两种是气态 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物比X的氢化物稳定 |
| D.Y与W元素的最高价氧化物对应的水化物的酸性比较,前者弱于后者 |
2012年,IUPAC正式命名了116号元素,下列关于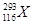 和
和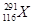 的说法中,错误的是
的说法中,错误的是
| A.这是两种原子 |
| B.两者电子数相差1 |
| C.两种原子中中子数分别为177和175 |
| D.两者互为同位素 |
现有四种短周期元素的原子半径及主要化合价数据如下表所示:
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子半径/nm | 0.186 | 0.102 | 0.152 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
下列叙述不正确的是
A.甲单质的熔点比丙单质的熔点高
B.甲单质可用电解其盐溶液的方法冶炼而得
C.常温下,丁的两种氢化物均为液体
D.乙的简单离子是四种元素各自形成的简单离子中半径最大的
下列有关叙述正确的是
A. O和 O和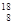 O中子数相同,质子数不同,互为同位素 O中子数相同,质子数不同,互为同位素 |
| B.H2O比H2S稳定,H-S键比H-O键更难断裂 |
| C.Na2O晶体中存在离子键,是离子化合物 |
| D.Na2O2晶体中阳离子与阴离子个数比为1:1 |