题目内容
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
| A.非金属性:T<X <R |
| B.气态氢化物稳定性:R <T<Q |
| C.R与Q的电子数相差16 |
| D.X与Q最高价氧化物的水化物的质子数相差18 |
D
解析试题分析:R单质在暗处与H2剧烈化合并发生爆炸,R为F元素,由元素在周期表中的位置可知,T为Cl元素,Q为Br元素,X为S元素,Z为Ar元素。A、Z为Ar元素,最外层为稳定结构,金属性与非金属性在同周期中最弱,同周期自左而右金属性减弱,故非金属性X<T<R ,故A错误;B、同主族自上而下,非金属性减弱,故非金属性F>Cl>Br,非金属性越强,气态氢化物越稳定,故稳定性HF>HCl>HBr,故B错误;C、R为F元素,Q为Br元素,原子序数相差26,故C错误;D、Q最高价氧化物的水化物为HBrO4质子总数为1+35+32=68,前者是硫酸,其质子总数为2+16+32=50,相差为18,故D正确;故选D。
考点:本题考查了结构位置性质关系、元素周期表的结构、元素周期律等,难度不大,推断R为氟元素是关键,注意掌握元素周期律。

练习册系列答案
相关题目
元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于负二价硫离子的半径,X元素为( )
| A.Al | B.P | C.Ar | D.K |
1863年提出原子学说,为近代化学发展奠定了坚实基础的化学家是( )
| A.英国的道尔顿 | B.法国的拉瓦锡 |
| C.俄国的门捷列夫 | D.英国的汤姆生 |
有X,Y两组原子,对它们结构的下列描述中,能说明彼此化学性质一定相似的是
| A.电子排布式分别为:1s2和1s22s2 |
| B.X原子M层上只有两个电子,Y原子N层上也只有两个电子 |
| C.X原子的2p亚层上有二对成对电子,Y原子的3p亚层上也有二对成对电子 |
| D.X原子的2p亚层上只有一个未成对电子,Y原子的3p亚层上只有一个未成对电子 |
铟产业被称为“信息时代的朝阳产业”。元素周期表中铟的数据见下图,下列说法完全正确的是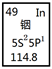
| A.铟元素的质量数是114.8 |
| B.铟元素的相对原子质量是114 |
| C.铟元素是一种主族元素 |
| D.铟原子最外层有3个能量相同的电子 |
以下比较中,正确的是 ( )
| A.微粒半径:F->O2->Na+>Li+ | B.电负性Cl>C ,酸性:HClO4>H2CO3, |
| C.分子中的键角:CH4>H2O>CO2 | D.稳定性:LiCl<NaCl<KCl<RbCl |