下列关于第IVA族元素的说法中,正确的是
| A.原子半径:14Si>32Ge |
| B.稳定性:CH4<SiH4 |
| C.酸性:H2CO3>H2SiO3 |
| D.碱性:32Ge(OH)4>50Sn(OH)4>82Pb(OH)4 |
X、Y、Z三种短周期元素在周期表中的位置如图所示,Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是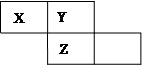
| A.气态氢化物的沸点:Z<Y |
| B.Z元素的氧化物对应的水化物一定是一种强酸 |
| C.三种元素原子半径的大小顺序为: X>Y>Z |
| D.Z单质与Fe反应生成的化合物中,铁元素显+3价 |
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化。图中纵坐标表示
| A.电子层数 | B.原子半径 | C.最高化合价 | D.最外层电子数 |
关于元素周期表的说法正确的是
| A.元素周期表中有8个主族 | B.元素周期表中有7个周期 |
| C.周期表中的主族都有金属元素 | D.IA族中的元素全部是金属元素 |
由短周期元素和长周期元素共同组成的族可能是
| A.主族 | B.副族 | C.Ⅷ族 | D.Ⅶ族 |
不同元素的原子间最本质的区别是
| A.中子数不同 | B.相对原子质量不同 |
| C.质子数不同 | D.最外层电子数不同 |
属于短周期元素的是
| A.K | B.Ca | C.I | D.P |
元素的性质呈周期性变化的根本原因是( )
| A.随着元素相对原子质量的递增,量变引起质变 |
| B.元素的原子半径呈周期性变化 |
| C.元素原子核外电子排布呈周期性变化 |
| D.元素的金属性和非金属性呈周期性变化 |
X、Y、Z、M、N代表五种金属,有以下化学反应:
①水溶液中:X+Y2+=X2++Y;
②Z+2H2O(冷)=Z(OH)2+H2↑;
③M、N为电极与N盐溶液组成原电池,负极反应为:M-2e-=M2+;
④Y可以溶于稀H2SO4中,M不能被H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
| A.M<N<Y<X<Z | B.N<M<Y<X<Z |
| C.N<M<X<Y<Z | D.X<Z<N<M<Y |
1863年提出原子学说,为近代化学发展奠定了坚实基础的化学家是( )
| A.英国的道尔顿 | B.法国的拉瓦锡 |
| C.俄国的门捷列夫 | D.英国的汤姆生 |