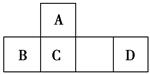
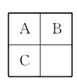
短周期元素甲、乙、丙、丁、戊的原子序数依次增大,甲是周期表中原子半径最小的元素,乙形成的气态氢化物的水溶液呈碱性,乙与丁同族,丙、丁、戊同周期,丙单质可制成半导体材料,戊的最高化合价为+7,则 ( )。
| A.原子半径:乙>丁>丙 |
| B.非金属性:丙>丁>戊 |
| C.甲与戊形成的化合物是共价化合物 |
| D.乙、丙、丁最高价氧化物对应的水化物均是强酸 |
Q、W、X、Y、Z都是短周期元素。X、Y、Q在周期表中的位置关系如图。W、Z的最外层电子数相同,Z的核电荷数是W的2倍。则下列说法不正确的是 ( )。
| ⅠA | ⅡA | ⅢA | ⅣA |
| | | | Q |
| X | | Y | |
A.非金属性:W>Z
B.原子半径:X>Y>Z
C.最高价氧化物对应水化物的碱性:X>Y
D.氢化物稳定性:Q>W
短周期元素甲、乙、丙、丁的原子序数依次增大。甲的最高价氧化物与乙的气态氢化物同时通入水中,得到的生成物既可与酸反应又可与碱反应。丙位于第ⅠA族,丁原子的核外电子总数是其最外层电子数的3倍,则 ( )。
| A.气态氢化物的稳定性:乙<丁 |
| B.原子半径:甲<乙 |
| C.丙的两种氧化物都是离子化合物 |
| D.甲、乙、丁的最高价氧化物对应的水化物酸性依次增强 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )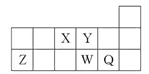
| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q) |
| C.离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| D.元素W的最高价氧化物对应的水化物的酸性比Q的强 |
根据中学化学教材所附元素周期表判断,下列叙述正确的是( )
| A.L电子层电子数为奇数的所有元素都是非金属 |
| B.第三、四、五、六周期元素的数目分别是8、18、32、32 |
| C.由左至右第8、9、10三列元素中没有非金属元素 |
| D.只有第ⅡA族元素的原子最外层有2个电子 |
X、Y、Z是三种短周期的主族元素,在周期表中的位置如图所示,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
| A.原子半径:Y>Z>X |
| B.气态氢化物的热稳定性:X<Z |
| C.Y和Z的最高价氧化物对应水化物均为强酸 |
| D.若Z的最高正价为+m,则X的最高正价也一定为+m |