根据元素周期律和物质结构的有关知识,以下有关排序错误的是( )
| A.离子半径:S2->Cl->Ca2+ | B.原子半径:Ca>S>Cl |
| C.酸性:HClO4<HBrO4<HIO4 | D.热稳定性:HCl>H2S>H2Se |
1913年,丹麦科学家玻尔第一次认识到氢原子光谱是氢原子的电子跃迁产生的。玻尔的原子结构理论一个很大的成就是( )。
| A.证明了原子核外电子在圆形轨道上运动 |
| B.提出了原子核是可以进一步细分的 |
| C.解决了氢原子光谱和原子能级之间的关系 |
| D.应用了量子力学理论中的概念和方法 |
下列说法正确的是( )。
| A.氢原子光谱是元素的所有光谱中最复杂的光谱之一 |
| B.“量子化”就是不连续的意思,微观粒子运动均有此特点 |
| C.玻尔理论不但成功解释了氢原子光谱,而且还推广到其他原子光谱 |
| D.原子中电子在具有确定半径的圆周轨道上像火车一样高速运转着 |
关于原子模型的演变过程,正确的是( )。
| A.汤姆逊原子模型→道尔顿原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型 |
| B.汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型→道尔顿原子模型 |
| C.道尔顿原子模型→卢瑟福原子模型→汤姆逊原子模型→玻尔原子模型→量子力学模型 |
| D.道尔顿原子模型→汤姆逊原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型 |
自从1803年英国化学家、物理学家道尔顿提出了原子假说,人类对原子结构的认识就不断深入、发展,并通过实验事实不断地完善对原子结构的认识。下列关于原子结构模型的说法中,正确的是( )。
| A.道尔顿的原子结构模型将原子看作实心球,故不能解释任何问题 |
| B.汤姆逊“葡萄干布丁”原子结构模型成功地解释了原子中的正负粒子是可以稳定共存的 |
| C.卢瑟福核式原子结构模型指出了原子核和核外电子的质量关系、电性关系及占有体积的关系 |
| D.玻尔电子分层排布原子结构模型引入了量子化的概念,能够成功解释所有的原子光谱 |
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示, 其中T单质和H2在光照的条件下发生爆炸。则下列判断正确的是
| A.五种元素中Z的活动性最弱,T 的氧化物对应水化合物酸性最强 |
| B.氢化物的稳定性:R>Q>X;R>T>X |
| C.Q单质能从溶液中置换出X单质,R单质能从溶液中置换出T单质 |
| D.X阴离子和T阴离子相比,半径:X阴离子的大;还原性:T阴离子的强 |
下列说法正确的是
| A.L层上的电子数为奇数的原子一定是主族元素的原子 |
| B.元素周期表共有18列,第8列属于第ⅧB族、第17列属于第VIIA族 |
| C.化学键的形成一定伴随着电子的转移和能量变化 |
| D.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素 |
X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20。下列判断正确的是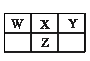
| A.四种元素的原子半径:rZ>rX>rY>rW |
| B.四种元素形成的单质最多有6种 |
| C.四种元素均可与氢元素形成电子总数为18的分子 |
| D.四种元素中,Z的最高价氧化物对应的水化物酸性最强 |
下列说法正确的是
| A.14C与14N互为同位素 | B.葡萄糖与果糖互为同分异构体 |
| C.H2与CH4互为同系物 | D.SO2与SO3互为同素异形体 |