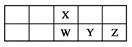
在短周期元素中,原子最外电子层只有1个或2个电子的元素是( )
| A.金属元素 | B.稀有气体元素 | C.非金属元素 | D.无法确定为哪一类元素 |
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A.元素X的常见化合价是+1
B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
已知1~18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2—>Z — |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
下列化合物中阴离子半径和阳离子半径之比最大的是 ( )
| A.LiI | B.NaBr | C.KCl | D.CsF |
元素周期律和元素周期表是学习化学的重要工具,下列说法不正确的是( )
| A.同周期的主族元素中,ⅦA族元素的原子半径最小 |
| B.碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 |
| C.元素周期表中从ⅢB到ⅡB十个纵列的元素都是金属元素 |
| D.ⅠA元素的原子,其半径越大,越容易失去电子 |
X、Y、Z为三种短周期元素,X、Y处在相邻的两个周期,X原子的最外层电子数是Y原子最外层电子数的2倍,Y的原子序数比X的原子序数多5,Z原子与Y原子的最外层电子数之差为3。下列叙述正确的是( )
| A.X、Y、Z三种元素不能组成一种盐 |
| B.X单质与Z单质直接反应可生成两种化合物 |
| C.X、Y、Z的最高价氧化物对应的水化物,可能是酸、碱或两性的物质 |
| D.X、Y形成的一种离子跟H+反应可生成Y的离子 |
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则对下列叙述的判断正确的是( )
①a-b=m-n
②元素的原子序数a>b>c>d
③元素非金属性Z>R
④最高价氧化物对应水化物的碱性X>Y
| A.②③ | B.③ | C.①②③④ | D.①②③ |
下列事实不能作为实验判断依据的是( )
| A.钠和镁分别与冷水反应,判断钠和镁的金属活动性强弱 |
| B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱 |
| C.硫酸和硅酸钠溶液反应出白色沉淀,判断硫与硅的非金属活动性强弱 |
| D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
下列有关化学用语使用正确的是( )
A.硫原子的原子结构示意图: |
B.NH4Cl的电子式: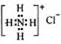 |
C.原子核内有10个中子的氧原子: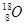 |
| D.纯碱的化学式为NaOH |