下列性质的比较正确的是
| A.酸性:H2SiO3>H2CO3 | B.碱性:Mg(OH)2>Al(OH)3 |
| C.稳定性:SiH4>PH3 | D.原子半径:N>C |
短周期主族元素X、Y、Z、W 的原子序数依次增大, X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法正确的是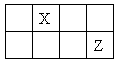
| A.原子半径: r(Y)> r (Z)> r (W) |
| B.Y、Z、W的简单离子的电子层结构相同 |
| C.XWm与YWn中化学键类型相同(m、n为正整数) |
| D.元素Z 的简单气态氢化物的热稳定性比W 的强 |
下列叙述正确的是( )
| A.越难失电子的元素得电子能力一定越强 |
| B.溶于水可以导电的化合物一定是离子化合物 |
| C.第三周期元素的最高正化合价等于它所处的主族序数 |
| D.离子化合物中可以含有共价键,共价化合物可以含有离子键 |
运用元素周期律分析下面的推断,其中错误的是( )
| A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体 |
| B.铍(Be)是一种金属,它的氧化物的水化物可能具有两性 |
| C.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
下列有关说法正确的是( )
| A.在多电子的原子里,能量高的电子通常在离核近的区域内运动 |
| B.最外层电子数为8的微粒均是稀有气体元素的原子 |
| C.俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D.在周期表中金属和非金属的分界线附近寻找制备半导体材料 |
下列叙述中错误的是( )
| A.原子半径:Na>Si>Cl | B.稳定性:SiH4<HCl<H2S |
| C.金属性:Na>Mg>Al | D.酸性:H3PO4<H2SO4<HClO4 |
元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为( )
| A.XY2 | B.X2Y3 | C.X3Y2 | D.XY2 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中不正确的是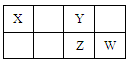
| A.Y与Z形成的化合物是形成酸雨的原因之一 |
| B.W的单质能与水反应,生成一种具有漂白性的物质 |
| C.最高价氧化物对应水化物的酸性:W >Z >X |
| D.气态氢化物的稳定性:W > Z >Y |
下列各微粒中,各个电子层电子数都达到2n2个的是
| A.Ne、Ar | B.Al3+、S2- | C.F-、Na+ | D.He、Cl- |
