已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A.离子半径:C>D>B>A | B.原子序数:d>c>b>a |
| C.原子半径:A>B>C>D | D.单质的还原性:A>B>D>C |
铊是超导材料的组成元素之一,铊在元素周期表中位于第六周期,与铝是同主族元素,元素符号是Tl。以下对铊的单质及其化合物的性质推断中,不正确的是( )
| A.铊是易导电的银白色金属 | B.铊能生成+3价的离子 |
| C.Tl3+的氧化能力比Al3+强 | D.氢氧化铊的碱性比氢氧化铝强 |
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是 ( )
| A.X2-的还原性一定大于Y- |
| B.由mXa+与nYb-得m+a = n-b |
| C.X、Y一定不是同周期元素 |
| D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | —— |
| 最低负价 | —— | -1 | —— | —— | -3 | -2 | |
A.元素X和Q形成的化合物中不可能含有共价键
B.X、Z、R的最高价氧化物的水化物之间可两两相互反应
C.R3-比Q2-更容易失去电子
D.M(OH)2的碱性比XOH的碱性强
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 最外层电子数是次外层的3倍 |
| Z | 短周期中,其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
A.原子半径:X > Y > M
B. 由X、M和氢三种元素不可能形成离子化合物
C.气态氢化物热稳定性:M > Y > X
D.Z、Q、M的最高价氧化物对应的水化物可以两两发生反应
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是( )
| A.原子半径:rW>rZ>rY>rX |
| B.含Y元素的盐溶液一定显酸性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
短周期元素X、Y、Z、W在周期表中相对位置如下图所示,Y元素在地壳中的含量最高。下列说法正确的是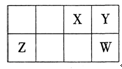
| A.原子半径:Z<Y<W |
| B.最简单气态氢化物的热稳定性:Y<W |
| C.含X的化合物形成的溶液一定呈酸性 |
| D.Y的最简单阴离子和Z的最简单阳离子核外电子数相同 |
XeF4在水中的反应为:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。下列说法中正确的是
| A.XeF4分子中各原子均达到8电子稳定结构 |
| B.XeF4分子中Xe的化合价为0价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2∶3 |
| D.XeF4按上述方式水解,每生成4molXe,转移16mol电子 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙是由X、Y、Z组成的盐。下列说法正确的是
| A.由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B.YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 |
| C.原子半径:Z<Y<W,而简单离子半径:W<Y<Z |
| D.W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
下列说法正确的是 ( )
| A.原子最外层电子数为2的元素一定处于周期表ⅡA族 |
| B.主族元素X、Y能形成XY2型化合物,则X与Y 的原子序数之差可能为2或5 |
| C.离子化合物中不可能存在共价键 |
| D.金属元素与非金属元素形成的化合物一定是离子化合物 |