以下是1-18号元素某性质的递变规律,Y轴代表的是 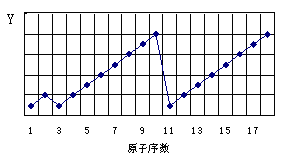
| A.原子半径 | B.金属性 | C.非金属性 | D.最外层电子数 |
已知短周期主族元素A、B在周期表中的相对位置如右图(稀有气体除外),则下列说法不正确的是
| | A |
| B | |
A.A一定是第2周期元素 B.B的原子半径一定比A大
C.B的金属性一定比A强 D.A的熔沸点一定比B高
下列事实一般不能用于判断金属性强弱的是( )
| A.金属的颜色和熔沸点 |
| B.金属元素的最高价氧化物对应的水化物的碱性强弱 |
| C.1mo金属单质在反应中失去电子的多少 |
| D.金属元素的单质和水或酸置换出氢的难易 |
列关于同主族元素的说法错误的是( )
| A.同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 |
| B.同主族元素随原子序数递增,单质氧化能力逐渐增强 |
| C.同主族元素原子最外层电子数都相同 |
| D.同主族元素的原子半径,随原子序数增大而逐渐增大 |
锗(Ge)是第四周期第IVA族元素,处于元素周期表中金属区与非金属区的交界线处,下列叙述正确的是( )
| A.锗是一种金属性很强的元素 | B.锗的单质具有半导体的性能 |
| C.锗化氢(GeH4)稳定性很强 | D.锗酸(H4GeO4)是难溶于水的强酸 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是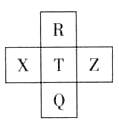
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
下列叙述中错误的是 ( )
| A.原子半径:Cl>S>O | B.还原性:Na>Mg>Al |
| C.稳定性:HF>HCl>HBr | D.酸性:HClO4>H2SO4>H3PO4 |
下列各组比较不正确的是 ( )
| A.锂与水反应不如钠与水反应剧烈 |
| B.还原性:K>Na>Li,故 |
| C.容沸点:Li>Na>K |
| D.原子半径:Li<Na<K |
下列叙述中正确的是( )
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.除短周期外,其他周期均有18种元素 |
| C.副族元素中没有非金属元素 |
| D.碱金属元素是指IA族的所有元素 |
对发现元素周期律贡献最大的化学家是 ( )
| A.牛顿 | B.道尔顿 | C.阿伏加德罗 | D.门捷列夫 |