X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
| 元素 | 相关信息 |
| X | X的一种核素的质量数为14,中子数为8 |
| Y | Y与X同周期,且它的一种氧化物只能用排水法收集 |
| Z | Z的单质常温下为黄绿色气体 |
| W | W的原子核外电子总数是其电子层数的4倍 |
A.原子半径:W> X>Y,离子半径:W>Z
B.氧化物对应的水化物的酸性:Z> Y>X
C.Y的最高正价含氧酸,可由它的氢化物为原料来制取
D.W的单质与X的一种氧化物不能发生置换反应
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是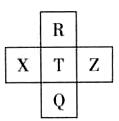
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
第三周期主族元素中,原子半径最大的是
| A.Na | B.Si | C.S | D.Cl |
相对原子质量原来以16O原子质量的十六分之一为标准,以该标准得到的仍为整数的是
| A.14N的质量数 | B.碳原子的相对质量 |
| C.氯元素的相对原子质量 | D.氢氧化钠的摩尔质量 |
3He月球上储量丰富,4He则来源于宇宙射线的初级粒子。下列关于3He和4He的说法正确的是
| A.两者互为同位素 | B.两者互为同素异形体 |
| C.两者为同一种原子 | D.两者具有相同的中子数 |
以下表述不符合元素周期律的是
| A.酸性:H3PO4>HNO3>HClO4 |
| B.热稳定性:HF>H2O>NH3 |
| C.离子半径:F->Na+>Mg2+ |
| D.还原性:HI>HBr>HCl |
下列各组原子中,化学性质一定相似的是
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅两个电子的Y原子 |
| C.2p轨道上只有一个空轨道的X原子与3p轨道上只有一个空轨道的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
下列叙述中,正确的是
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.如果某一基态原子3p轨道上仅有2个电子,它们自旋方向必然相反 |
| D.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
短周期元素X、Y、Z在元素周期表中的位置如图所示,其中Y与Z的原子最外层电子数之比为2:1.下列说法不正确的是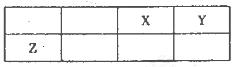
| A.X与Y只能形成两种化台物 |
| B.简单离子的半径大小:Y<X |
| C.X、Y、Z三种元素形成的化合物中既存在共价键又存在离子键 |
| D.Z形成的简单离子是其所在周期元素形成的简单离子中半径最小的 |