题目内容
X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
| 元素 | 相关信息 |
| X | X的一种核素的质量数为14,中子数为8 |
| Y | Y与X同周期,且它的一种氧化物只能用排水法收集 |
| Z | Z的单质常温下为黄绿色气体 |
| W | W的原子核外电子总数是其电子层数的4倍 |
A.原子半径:W> X>Y,离子半径:W>Z
B.氧化物对应的水化物的酸性:Z> Y>X
C.Y的最高正价含氧酸,可由它的氢化物为原料来制取
D.W的单质与X的一种氧化物不能发生置换反应
C
解析试题分析:由X的信息,质量数为14,中子数为8,可知质子数为6,为C;根据Y的信息,只能用排水法收集的氧化物当为NO,Y为N;Z信息对应的是Cl;W信息可设周期数为2时,对应的核外电子总数为8,即是O, 周期数为3时,对应的核外电子总数为12,即是Mg,所以W可为O或Mg;A.原子半径:C>N>O,离子半径Z>W,错误;B.应当表述为最高价氧化物对应的水化物的的酸性,错误;C.Y的最高正价含氧酸为HNO3,可以用氨氧化的方法来制取,正确;D.2Mg+CO2=(点燃)2MgO+2C,错误。
考点:质量数、中子数、质子数的关系;氮及其化合物的性质;镁的性质;二氧化碳的性质。

下列中各组性质的比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②离子还原性:S2->Cl->Br ->I- ③沸点:HF>HCl>HBr>HI
④金属性:K>Na>Mg>Al ⑤气态氢化物稳定性:HF>HCl>H2S ⑥半径:O2->Na+>Na>Cl
| A.①②③ | B.②③④ | C.①④⑤ | D.①②③④⑤⑥ |
下列各组物质中互为同位素的是 ( )
A. 和 和 | B.D和T | C.H2O和H2O2 | D.O3和O2 |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
| A.R的原子半径比Z的大 |
| B.R的氢化物的热稳定性比W的强. |
| C.X与Y形成的化合物只有一种 |
| D.Y的最高价氧化物的水化物的酸性比W的强 |
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中Y所处的周期序数与主族序数之和为8。下列说法错误的是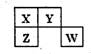
| A.Z元素的氧化物对应水化物的酸性一定弱于W |
| B.四种元素中Z的原子半径和形成的离子半径均最大 |
| C.X、Z、W中最简单气态氢化物稳定性最弱的是Z |
| D.X、Y、Z的原子均能与氢原子形成四原子分子 |
短周期元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期。下列推测正确的是
| A.元素Y的最高化合价为+7 |
| B.三种元素的原子半径rZ>rY>rX |
| C.Z的单质比Y的单质更易与H2反应 |
| D.化合物X2Z2中阴阳离子数之比为1: 2 |
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:
HXO4>H2YO4>H3ZO4,则下列判断中正确的是
| A.元素非金属性按X、Y、Z的顺序减弱 |
| B.原子的电子能力按X、Y、Z的顺序增强 |
| C.气态氢化物的稳定性按X、Y、Z的顺序增强 |
| D.单质的氧化性按X、Y、Z的顺序增强 |
下列叙述中正确的是
| A.卤素单质与水反应均可用X2+H2O===HXO+HX表示 |
| B.从F2到I2,卤素单质的颜色随着相对分子质量的增大而加深 |
| C.熔、沸点:Li>Na>K |
| D.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠 |