卤素间形成的化合物如“IF5、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应不正确的是( )
| A.IF5 + 3H2O = HIO3 +5HF |
| B.3IBr +2Fe = FeI3 + FeBr3 |
| C.BrCl的氧化性强于I2 |
| D.IBr可以与NaOH溶液反应生成2种盐 |
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:HXO4>H2YO4>H3ZO4,则下列判断中正确的是( )
| A.元素非金属性按X、Y、Z的顺序减弱 |
| B.原子的电子能力按X、Y、Z的顺序增强 |
| C.气态氢化物的稳定性按X、Y、Z的顺序增强 |
| D.单质的氧化性按X、Y、Z的顺序增强 |
有人建议将氢元素排在元素周期表的第ⅦA族。下列事实能支持这一观点的是( )
①氢原子得到一个电子后最外层电子达到稳定结构 ②氢分子的结构式为H—H
③与碱金属元素形成离子化合物M+[∶H]- ④分子中原子间的化学键都属于非极性键
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
下图是元素周期表前四周期的一部分,关于元素R、W、X、Y、Z的叙述正确的是( )
| A.最高价氧化物的水化物的酸性:W>Y |
| B.Z的单质常温下是液体,所在的周期中含有32种元素 |
| C.Z的原子序数比R大17 |
| D.氢化物的沸点:X<Z |
已知1~18号元素的离子aW3+、bX+、cY2-、dZ - 都具有相同的电子层结构,下列关系正确的是( )
| A.离子的还原性:Y2->Z- | B.质子数:c>b |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
2014年5月7日南京某建设公司丢失用于材料探伤的放射源Ir—192(铱—192)一枚,经相关部门的努力追查,丢失的放射源于5月10日被回收,Ir—192的放射性会对人体产生很大的伤害。已知Ir元素位于周期表中第6周期第Ⅷ族,原子序数为77,192为该核素的质量数,下列关于Ir—192的说法正确的是( )
| A.Ir—192核外含有115个电子 | B.Ir为非金属元素 |
| C.Ir—192中子数与质子数的差为38 | D.Ir元素与碘元素位于同一周期 |
关于919F-微粒叙述正确的是( )
| A.质量数为19,电子数为9 | B.质子数为9,中子数为10 |
| C.质子数为9,电子数为9 | D.中子数为10,电子数为8 |
根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
 A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<QC.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
短周期元素X、Y、Z在元素周期表中的位置下图所示,下列说法正确的是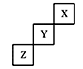
| A.X、Y、Z三种元素中,单质在常温下均为气态 |
| B.Z的氢化物的稳定性比Y的强 |
| C.Y的最高正化合价为+5 |
| D.Y的单质的熔点比Z的低 |