下列顺序表述正确的是
| A.酸性:H3PO4> HNO3> HClO4 | B.稳定性:H2O > HF > H2S |
| C.原子半径:Na > Mg > O | D.还原性:F-> Cl-> S2- |
下列叙述错误的是
| A.13C 和14C属于同种元素,它们互为同位素 |
| B.1H和2H是不同的核素,它们的质子数相等 |
| C.14C和14N的质量数相等,它们的中子数不等 |
| D.6Li和7Li的电子数相等,它们的中子数也相等 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )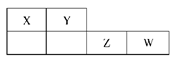
| A.氢化物稳定性:X>Y |
| B.最高价氧化物对应的水化物的酸性:W>Y |
| C.4种元素的单质中,W单质的熔、沸点最高 |
| D.干燥的W单质具有漂白性 |
下图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( )
| | | | a |
| | b | | |
| c | | d | |
| e | | | |
A.元素b位于ⅥA族,有+6、-2两种常见化合价
B.五种元素中,元素e的性质最稳定
C.原子半径有d>c>b
D.元素e参与形成的化合物可以作为一种半导体材料
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
| A.XYZ2 | B.X2YZ3 | C.X2YZ2 | D.XYZ3 |
某元素原子价电子构型3d54s2,其应在( )
| A.第四周期ⅡA族 | B.第四周期ⅡB族 |
| C.第四周期ⅦA族 | D.第四周期ⅦB族 |
下列有关说法不正确的是( )
| A.C3H8中碳原子都采用的是sp3杂化 |
| B.O2、CO2、N2都是非极性分子 |
| C.酸性:H2CO3<H3PO4<H2SO4<HClO |
D.CO的一种等电子体为NO+,它的电子式为 |
下列说法或有关化学用语的表达正确的是( )
| A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B.基态Fe原子的外围电子排布图为: |
| C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
某元素原子的质量数为52,中子数为28,其基态原子未成对电子数为( )
| A.1 | B.3 | C.4 | D.6 |