海水提镁的主要流程如下: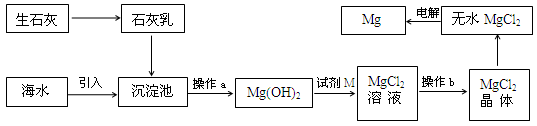
下列说法正确的是
①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应
③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量
| A.①②③④⑤ | B.②③ | C.④⑤ | D.①④⑤ |
部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理: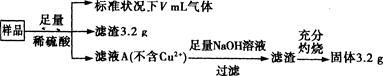
下列说法正确的是 ( )
| A.滤液A中的阳离子为Fe3+、Fe2+、H+ |
| B.V=896 |
| C.样品中CuO的质量为4.0 g |
| D.样品中Fe元素的质量为2.24g |
海水的综合利用可以制备金属钠和镁等,其流程如下图所示:
下列说法不正确的是 ( )
| A.海水提盐都属于物理变化 |
| B.利用母液可进一步提取溴,但要富集 |
| C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+ |
| D.不用电解MgO来制取镁是因为MgO熔点高,能耗大 |
溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32?、SO42?、NO3?中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如下图所示。则下列说法正确的是( )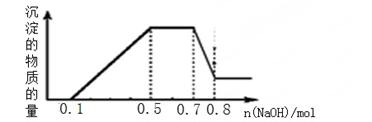
| A.溶液中一定不含CO32?,可能含有SO42?和NO3? |
| B.在滴加NaOH溶液物质的量为0.5至0.7mol时,发生的离子反应为:Al3++4OH-=[Al(OH)4]- |
| C.溶液中的阳离子只有H+、Mg2+、Al3+ |
| D.n(H+)∶n(NH4+)∶n(Mg2+) =2∶4∶1 |
25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) △H2=-511kJ·mol-1
下列说法正确的是( )
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa下,Na2O2(s)+2Na(s)=2Na2O(s) △H=-317kJ·mol-1 |
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色→①变灰暗→②变白色→③出现液滴→④白色固体,下列说法中正确的是 ( )
| A.①发生了氧化还原反应 | B.②变白色是因为生成了碳酸钠 |
| C.③是碳酸钠吸收空气中的水蒸气形成了溶液 | D.④只发生物理变化 |
下列说法中不正确的是 ( )
| A.向滴有酚酞的水中加入过量Na2O2粉末并振荡,溶液由无色变红又变无色 |
| B.向包有Na2O2粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明Na2O2与H2O反应是一个放热反应且有氧气生成 |
| C.Na2O2与H2O反应是一个氧化还原反应,Na2O2既是氧化剂,又是还原剂 |
| D.Na2O2与H2O反应是一个置换反应,有单质O2产生 |
下列关于Na2O2的叙述,正确的是 ( )
| A.Na2O2晶体中的阴离子与阳离子的物质的量之比为1:1 |
| B.Na2O2晶体为离子晶体,且含极性共价键 |
| C.Na2O2应保存于密封、干燥带玻璃塞的广口瓶中 |
| D.Na2O2与盐酸反应,不仅有盐和水生成,同时会放出无色气体 |
铝能用来冶炼难熔金属(如Fe 、V、Mn等),这是因为铝有
| A.两性 | B.良好导电性 |
| C.熔点低 | D.还原性,在反应中放出大量热 |