题目内容
部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法正确的是 ( )
| A.滤液A中的阳离子为Fe3+、Fe2+、H+ |
| B.V=896 |
| C.样品中CuO的质量为4.0 g |
| D.样品中Fe元素的质量为2.24g |
D
解析试题分析:A. 由于氧化性Fe3+>Cu2+>H+,铁离子优先反应,所以滤液中一定不存在铁离子,故A错误;B由于部分铁用于置换金属铜,则与氢离子反应生成氢气的铁的物质的量小于0.04mol,反应生成的气体的物质的量小于0.04mol,标况下生成的气体的体积一定小于:22.4mol/L×0.04mol=0.896L=896mL,故B误;C选项由于生成了氢气、滤液中不含铜离子,滤渣3.2g为金属铜,铜元素的物质的量为0.05mol,若全部为氧化铜,氧化铜的质量为:80g/mol×0.05mol=4.0g,由于部分铜被氧化成氧化铜,则样品中氧化铜的质量一定小于4.0g,故C错误;D选项滤液A中含有亚铁离子和氢离子,加入足量氢氧化钠溶液后,过滤,最后灼烧得到的固体为氧化铁,3.2g氧化铁的物质的量为0.02mol,含有铁元素的物质的量为0.02mol×2=0.04mol,样品中所有铁元素都生成了氧化铁,所以样品中Fe元素的质量为:56g/mol×0.04mol=2.24g,故D确;
考点: 考查了铁、铜单质及其氧化物的性质的相关知识点。

 阅读快车系列答案
阅读快车系列答案硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
I.对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是 。
| 第1组 | 第2组 | 第3组 |
| S (单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、 NaHSO4 |
Ⅱ.某校化学学习小组用下图所示的实验装置研究SO2气体还原Fe3+、Br2的反应。
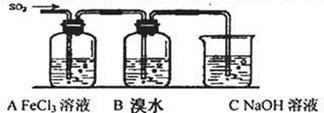
(1)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热的浓硫酸
(2)装置C的作用是除去多余的SO2,防止污染空气。已知在用氢氧化钠溶液吸收SO2的 过程中,往往得到Na2SO3和NaHSO3的混合溶液,常温下,溶液pH随n(SO32—):n(HSO3—)变化关系如下表
| n(SO32—):n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
当吸收液中n(SO32—):n(HSO3—) =10:1时,溶液中离子浓度关系正确的是 。
A.c(Na+)+ c(H+)= 2c(SO32—)+ c(HSO3—)+ c(OH—)
B.c(Na+)>c(HSO3—)>c(SO32—)>c(OH—)>c(H+)
C.c(Na+)>c(SO32—)>c(HSO3—)>c(OH—)>c(H+)
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中反应后的溶液分成三份,并设计了如下探究实验,请你评价并参与他们的探究过程(限选试剂:KMnO4溶液、KSCN溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝 酸、Ba(NO3)2溶液、新制的氯水)
| 序号 | 实验方案 | 实验现象 | 结论 |
| 方案① | 往第一份试液中加入KMnO4溶液溶液 | 紫红色褪去 | SO2与Fe3+反应生成了Fe2+ |
| 方案② | 往第二份试液中加入 | | SO2与Fe3+反应生成了Fe2+ |
| 方案③ | 往第二份试液中加入 | | SO2与Fe3+反应生成了SO42— |
上述方案①得出的结论是否合理 ,原因 。
如果他们设计的方案②与方案③均合理并且得到相应结论,请你将上面表格补充完整。
(4)装置B中能表明Br—的还原性弱于SO2的现象是 。
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色→①变灰暗→②变白色→③出现液滴→④白色固体,下列说法中正确的是 ( )
| A.①发生了氧化还原反应 | B.②变白色是因为生成了碳酸钠 |
| C.③是碳酸钠吸收空气中的水蒸气形成了溶液 | D.④只发生物理变化 |
为了使AlCl3溶液中的Al3+离子尽可能全部转化为Al(OH)3沉淀,最合适的试剂是
| A.NaOH溶液 | B.KOH溶液 | C.盐酸 | D.氨水 |
如图所示,甲、乙、丙、丁分别代表Na2CO3、NaOH、NaHCO3、CO2四种物质,a、b、c、d、e、f分别表示两种物质间的转化关系。对于图中两种物质间的转化,通过一步反应就能实现的有
| A.只有a、b、c、d | B.只有b、c、d、e |
| C.只有c、d、e、f | D.a、b、c、d、e、f |
科学家研制出了一种新型的贮氢材料——镁铝合金。这种镁铝合金具有特定的组成,其成分可表示为Mg17Al12。其贮氢和释氢的原理可表示为:Mg17Al12+17H2  17MgH2+12Al
17MgH2+12Al
下列有关说法正确的是( )
| A.该合金的熔点介于镁和铝的熔点之间 |
| B.Mg17Al12是离子化合物 |
| C.732g的合金能吸收380.8L氢气 |
| D.熔炼制备Mg17Al12时需通入氩气,目的是防止金属被氧化 |
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为 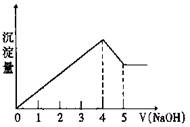
| A.2∶1 | B.4∶1 | C.1∶1 | D.1∶2 |