氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是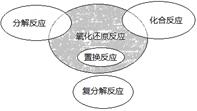
| A.4NH3 +5O2 =4NO+6 H2O |
| B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.2NaHCO3=Na2CO3+H2O+CO2↑ |
| D.Cl2+2NaBr=2NaCl +Br2 |
下列反应属于氧化还原反应,但水既没有做氧化剂又没有做还原剂的是
| A.2F2+2H2O ="4HF" +O2 |
| B.3NO2+H2O =2HNO3+NO |
| C.2Na +2H2O=2NaOH+H2 |
| D.CaO+H2O =Ca(OH)2 |
新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下: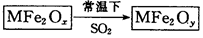
则下列判断正确的是( )
| A.x>y | B.MFe2Ox是还原剂 |
| C.SO2是该反应的催化剂 | D.SO2发生了置换反应 |
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
| A.135 L | B.90 L | C.168 L | D.157 L |
工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的伤害,必须进行处理。该法的工艺流程为
其中第①步存在平衡:2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O下列说法错误的是
Cr2O72—(橙色)+H2O下列说法错误的是
| A.在第①反应平衡体系中加入水,溶液中c(H+)增大 |
| B.溶液的pH值不变时,说明第①步反应达平衡状态 |
| C.第②步中,还原0.01mol Cr2O72—离子,需要0.06mol的FeSO4·7H2O。 |
| D.上述三步转化反应中,只有一个反应为氧化还原反应 |
下列变化中,需加氧化剂才能实现的是
| A.NaClO →NaCl | B.Na2O2 → O2 | C.C → CO2 | D.CaO→Ca(OH)2 |
分类是常用的学习方法,对于反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑的分类错误的是
| A.化合反应 | B.氧化还原反应 | C.离子反应 | D.放热反应 |
下列叙述中正确的是
| A.氧化还原反应的实质是元素化合价的升降 |
| B.非金属元素从化合态变为游离态时,该元素一定被氧化 |
| C.氧化剂氧化其他物质时本身一定被还原 |
| D.具有氧化性的物质在反应中一定做氧化剂 |
下列实验现象与氧化还原反应有关的是
| A.SO2通入品红溶液中,溶液褪色 |
| B.新制氯水密闭放置一段时间后浅黄绿色消失 |
| C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
| D.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO△ 3Cu+N2+3H2O,对此反应的分析合理的是
| A.该反应属置换反应 |
| B.NH3被氧化为N2 |
| C.反应体现了金属铜的还原性 |
| D.每生成1mol H2O 就伴随着1mol电子转移 |