日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B.用石膏粉制作石膏雕像 |
| C.用铝质或铁质容器盛放浓硝酸 |
| D.酸雨的形成 |
下列反应既属于氧化还原反应,又是吸热反应的是
| A.灼热的碳与CO2的反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.铝片与稀盐酸的反应 | D.甲烷在氧气中的燃烧反应 |
对于铝热反应:Fe2O3 + 2Al 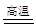 2Fe + Al2O3,下列说法中正确的是( )
2Fe + Al2O3,下列说法中正确的是( )
| A.Fe元素的化合价升高 | B.若27 g Al参加反应则有3 mol电子转移 |
| C.Fe2O3发生氧化反应 | D.Al被还原 |
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
| A.2Na2O2+2H2O =4NaOH+O2↑ | B.Cl2 + H2O  HClO + HCl HClO + HCl |
| C.2F2+2H2O=4HF+O2 | D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
下列有关氧化还原反应的叙述正确的是
| A.在一定条件下能发生反应:3O2=2O3,该反应不属于氧化还原反应 |
| B.氧化反应一定先于还原反应发生 |
| C.氧化性强的物质与还原性强的物质接触一定能发生反应 |
| D.氧化剂本身一定只发生还原反应 |
从淡化海水中提取溴的流程如图所示,下列有关说法错误的是 ( )。
| A.X为SO2气体,也可将SO2换成Na2SO3 |
| B.设备Y为蒸馏塔 |
| C.在提取溴的过程中一定有Br-被氧化 |
| D.工业上每获得1 mol Br2,需要消耗Cl2的体积最多为44.8 L(标准状况下) |
根据表中信息,判断下列叙述中正确的是 ( )。
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为2MnO4—+5H2O2+6H+=2Mn2++5O2↑+8H2O
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125 ℃分解为LiH、H2和Al。下列叙述错误的是( )。
| A.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
| B.LiAlH4与D2O反应,所得氢气的摩尔质量为4 g·mol-1 |
| C.1 mol LiAlH4在125 ℃完全分解,转移3 mol电子 |
| D.LiAlH4与水反应生成三种物质时,化学方程式可表示为:LiAlH4+4H2O=Al(OH)3+LiOH+4H2↑ |
将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2Cr2O7溶液,发生的两个化学反应为:SO2+2Fe3++2H2O=SO42—+2Fe2++W ①
Cr2O72—+aFe2++bH+―→Cr3++Fe3++H2O ②。
下列有关说法正确的是( )。
| A.还原性:Cr3+>SO2 |
| B.方程式②中,a=6,b=7 |
| C.Cr2O72—能将Na2SO3氧化成Na2SO4 |
| D.方程式①中W为OH- |