题目内容
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
①2Na2O2+2H2O=4NaOH+O2↑
②4Fe(OH)2+O2+2H2O=4Fe(OH)3
③2F2+2H2O=4HF+O2
④2Al+2NaOH+2H2O=2NaAlO2+3H2↑
| A.①② | B.②③ | C.①③ | D.③④ |
D
解析

练习册系列答案
相关题目
一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应
 下列说法正确的是
下列说法正确的是
| A.CH3OH被氧化,表现氧化性 |
| B.此条件下还原性强弱为:N2>CH3OH |
| C.若氧化产物比还原产物多0.2 mol,则该反应中转移3 mole- |
| D.该反应过程中断裂的化学键既有极性键又有非极性键 |
下列有关氧化还原反应的叙述正确的是
| A.在一定条件下能发生反应:3O2=2O3,该反应不属于氧化还原反应 |
| B.氧化反应一定先于还原反应发生 |
| C.氧化性强的物质与还原性强的物质接触一定能发生反应 |
| D.氧化剂本身一定只发生还原反应 |
某国外化学教材中有一张关于氧化还原反应的插图:由图可知,在该反应中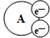 是
是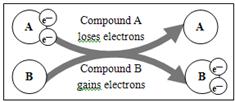
| A.还原剂 | B.氧化剂 | C.氧化产物 | D.还原产物 |
化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是
| A.氮肥厂用氮气和氢气合成氨气 | B.硝酸厂用氨氧化法制硝酸 |
| C.从海水中提溴 | D.纯碱厂用NaCl、NH3、CO2等制纯碱 |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是( )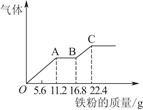
| A.原混合酸中NO物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol/L |
下列说法正确的是( )
| A.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA |
| B.化合反应均为氧化还原反应 |
| C.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
| D.易燃试剂与强氧化性试剂分开放置并远离火源 |
亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害。其在酸性条件下会产生NO和NO2。下列有关说法错误的是( )
| A.NaNO2既具有氧化性又具有还原性 |
| B.食用“醋溜豆芽”可能会减少亚硝酸钠对人体的危害 |
C.NaNO2和胃酸作用的离子方程式为: |
| D.1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol |
下列说法正确的是( )。
| A.反应Na→Na2O→Na2O2中钠元素被连续氧化 |
| B.1 mol金属钠发生反应Na→Na2O和发生反应Na→Na2O2转移电子数相等 |
| C.1 mol Cl2与足量Fe反应转移3 mol电子 |
| D.将1 mol Cl2通入1 L水中转移的电子为1 mol |