某金属和硝酸反应,已知参加反应的被还原的硝酸和参加反应的硝酸的物质的量之比为1∶6,若已知还原产物唯一,则还原产物为
| A.N2 | B.N2O | C.NO | D.NO2 |
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3—、Fe2+、NH4+、H+、H2O,下列叙述正确的是
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1mol NO3—发生氧化反应,转移电子5mol |
| D.若将该反应设计成原电池,则负极反应为Fe3++e—=Fe2+ |
已知Cu+在酸性条件下能发生下列反应:Cu+ → Cu + Cu2+(未配平)。NH4CuSO3与足量的10mol·L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②有刺激性气味气体产生 ③溶液呈蓝色。据此判断下列说法一定合理的是
| A.气体是二氧化硫 | B.NH4CuSO3中铜元素全部被氧化 |
| C.反应后为硫酸铜溶液 | D.硫酸全部作氧化剂 |
向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L。若将该混合物加入500mL14 mol·L-1的HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体?(假设浓度小于9mol/L为稀HNO3)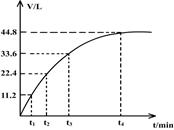
| A.t1 | B.t2 | C.t3 | D.t4 |
根据表中信息判断,下列选项正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… |
| ② | C12、FeBr2 | FeC13、FeBr3 |
| ③ | MnO4-…… | C12、Mn2+…… |
A.第①组反应的其余产物为H2O
B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1:2
C.第③组反应中生成lmol Cl2,转移电子5mol
D.氧化性由强到弱顺序为MnO4一>Cl2> Fe3+> Br2
科学家最近用金属钠还原CCl4和SiCl4制得一种一维SiC纳米捧。相关反应的化学方程式为:8Na+CCl4十SiCl4=SiC十8NaCl。下列说法不正确的是( )
| A.一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力 |
| B.上述反应中SiC既是氧化产物又是还原产物 |
| C.SiCl4是由极性键构成的非极性分子 |
| D.CCl4分子、SiCl4分子、SiC晶体中各原子都达到了8电子稳定结构 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是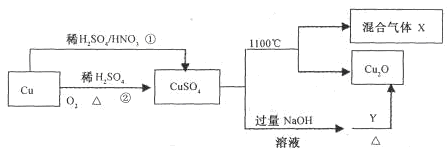
| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1 mol |
| D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
去年下半年我省雾霾天气十分严重。PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO—催化剂→N2+CO2,下列关于此反应的说法中,不正确的是
| A.所涉及元素的第一电离能:N>O>C |
| B.当x=2时,每生成1molN2,转移电子数为4mol |
C.等物质的量N2和CO2中,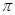 键的个数比为1:1 键的个数比为1:1 |
| D.氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
下列说法中正确的是( )
| A.含有金属元素的离子一定是阳离子,金属阳离子被还原一定得到金属单质 |
| B.pH相等的NaOH、NaHCO3和Na2CO3三种溶液: c(NaOH)<c(NaHCO3)<c(Na2CO3) |
| C.常温下,c(NH4+)相等的4种溶液:①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl ④(NH4)2CO3,溶质物质的量浓度大小关系是:②<①<④<③ |
| D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液pH=2,则a:b=2:9 |
下列叙述正确的是( )
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.用乙烷(CH3CH3)或乙烯(CH2=CH2)制一氯乙烷(CH3CH2Cl)的反应类型相同 |
| C.煤油是通过煤干馏获得,可用作燃料和保存少量金属钠 |
D.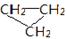 和CH3-CH=CH2互称为同分异构体 和CH3-CH=CH2互称为同分异构体 |