题目内容
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3—、Fe2+、NH4+、H+、H2O,下列叙述正确的是
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1mol NO3—发生氧化反应,转移电子5mol |
| D.若将该反应设计成原电池,则负极反应为Fe3++e—=Fe2+ |
A
解析试题分析:从以上的反应物和生成物上分析,NO3—、Fe2+、H+是反应物,Fe3+、NH4+、H2O是生成物。 A、Fe(NO3)2溶液若加酸酸化将被氧化为Fe(NO3)3,正确;B、根据得失电子守恒,氧化剂NO3—得8个电子成为NH4+,还原剂失1个电子成为Fe3+,所以氧化剂与还原剂的物质的量之比为1:8,错误;C、若有1mol NO3—发生氧化反应,则转移电子8mol,错误;D、若将该反应设计成原电池,负极发生氧化反应,应为Fe2+-e-= Fe3+,错误,答案选A。
考点:考查氧化还原反应有关知识

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。
实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KIO3溶液;
实验Ⅱ:在一定量的KIO3溶液中逐滴加NaHSO3溶液。下列说法正确的是
| A.两个实验中溶液的pH变化趋势相同 |
| B.两实验中生成等量I2时,转移电子数的物质的量相同 |
| C.在实验Ⅰ的过程中,若NaHSO3初始量为3mol,当溶液中I¯与I2的物质的量之比为5∶2时,氧化产物为3.2mol |
| D.过程Ⅱ中,可以用淀粉作为滴定指示剂,判定第一阶段的反应终点 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是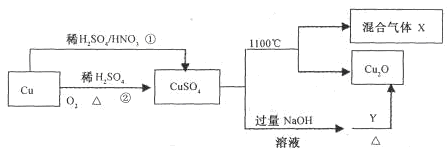
| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1 mol |
| D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
科技工作者提出用铝粉处理含亚硝酸盐废水的思路:调节亚硝酸盐废水酸碱性,使其pH>12,然后加入适量的铝粉、搅拌,从而实现预期且的。下列判断错误的是
| A.废水处理时铝单质转化为Al3+ | B.废水处理中,亚硝酸盐被还原 |
| C.处理过程中,OH一参与了反应 | D.铝粉颗粒大小影响废水处理的速率 |
下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①O3+2KI+H2O=2KOH+I2+O2 ②SiO2+2C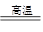 Si+2CO↑
Si+2CO↑
③SiO2+3C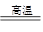 SiC+2CO↑ ④4HCl(浓)+MnO2
SiC+2CO↑ ④4HCl(浓)+MnO2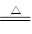 MnCl2+Cl2↑+2H2O( )
MnCl2+Cl2↑+2H2O( )
| A.仅有② | B.②④ | C.②③④ | D.①②③④ |
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2 Si3N4+6CO。下列叙述正确的是( )
Si3N4+6CO。下列叙述正确的是( )
| A.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂 |
| B.上述反应中每生成1 mol Si3N4,N2得到12 mol电子 |
| C.若已知上述反应为放热反应,升高温度,其平衡常数增大 |
| D.若使压强增大,上述平衡向正反应方向移动 |
有如下反应:①H2S+H2O2=S↓+2H2O
②S+O2=SO2 ③SO2+Br2+H2O=HBr+H2SO4
下列物质的氧化性强弱判断正确的是( )
| A.H2O2>S O2>SO2 | B.H2O2>O2 Br2>O2 |
| C.Br2>H2O2 SO2>S | D.Br2>H2O2 Br2>SO2 |
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是( )
| A.2Na2O2+2CO2=2Na2CO3+O2 | B.2NaHCO3=Na2CO3+H2O+CO2↑ |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 | D.Cl2+2KBr=Br2+2KCl |
在碘酸钠(NaIO3)的碱性溶液中通入氯气,可以得到高碘酸钠(Na2H3IO6)。下列有关该反应的说法错误的是 ( )。
| A.在该反应中碘酸钠作还原剂 |
| B.碱性条件下,氯气的氧化性强于高碘酸钠的氧化性 |
| C.反应中生成1 mol Na2H3IO6转移2 mol电子 |
| D.反应中氧化产物与还原产物的物质的量之比为2∶1 |