火法炼铜首先要焙烧黄铜矿,反应为:2CuFeS2+O2→Cu2S+2FeS+SO2 则下列说法正确的是
| A.CuFeS2仅作还原剂,硫元素被氧化 |
| B.每生成1mol Cu2S,有4 mol硫被氧化 |
| C.SO2只是氧化产物,FeS只是还原产物 |
| D.每转移1.2 mol电子,有0.2 mol硫被氧化 |
已知:① 向KMnO4晶体滴加浓盐酸,产生黄绿色气体;② 向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③ 取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝。下列判断正确的为
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
下列反应中转移电子的物质的量不等于2 mol的是
| A.1 mol Al与含1mol H2SO4的稀硫酸溶液反应 |
| B.1mol Cu与含4mol HNO3的稀硝酸溶液反应 |
| C.1 mol MnO2与含2 mol H2O2的双氧水反应 |
| D.1 mol Cu与含2 mol H2SO4的浓硫酸共热 |
下列所用的酸在反应中同时表现酸性和氧化性的是
| A.用浓盐酸与KMnO4反应制取Cl2 |
| B.向蔗糖中加入浓H2SO4,固体变黑膨胀 |
| C.用稀硫酸与CuO反应制取胆 |
| D.用浓硝酸除去铝表面的铜镀层 |
常温,下列气体不能共存且发生的反应属于非氧化还原的是
| A.NO和O2 | B.SO2和H2S |
| C.NH3和HCl | D.Cl2和SO2 |
科学家最近研究出一种环保,安全的储氢方法,其原理可表示为:
NaHCO3+H2 HCOONa+H2O,下列有关说法不正确的是( )
HCOONa+H2O,下列有关说法不正确的是( )
| A.储氢、释氢过程均有能量变化 |
| B.NaHCO3、HCOONa均含有离子键和共价键 |
| C.储氢过程中,NaHCO3被还原 |
| D.释氢过程中,每消耗0.1mol H2O放出2.24L的H2 |
在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应。下列说法正确的是
A.当x ≤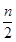 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- 时,反应的离子方程式为:2Fe2++ Cl2 → 2Fe3++ 2Cl- |
| B.当x ≥ n时,反应的离子方程式为:2Fe2++ 2I-+ 2Cl2 → 2Fe3++ I2+ 4Cl- |
| C.当Fe2+和I-同时被氧化时,x与n的关系为x>n |
| D.当x=n时,反应后氧化产物的物质的量为n mol |
已知粗碘中含有的IBr和ICl受热都会升华,若先在粗碘中加入下列物质中的一种再加热,就可制得纯净的碘。该物质是
| A.KI | B.H2O | C.Zn | D.NaCl |
吸进人体内的氧有2%转化为加速人体衰老的氧化性极强的活性氧,若Na2SeO3能清除人体内活性氧,则Na2SeO3的作用是
| A.还原剂 | B.氧化剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |
有Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述中,不正确的是
| A.还原产物为NH4+ |
| B.氧化剂与还原剂的物质的量之比为1∶8 |
| C.若有0.5mol NO3-参加还原反应,则转移电子8mol |
| D.若把该反应设计为电解池,则阳极反应为Fe2+-e→Fe3+ |