(4分)(2012?广东)下列应用不涉及氧化还原反应的是( )
| A.Na2O2用作呼吸面具的供氧剂 |
| B.工业上电解熔融状态的Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.实验室用NH4Cl和Ca(OH)2制备NH3 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.60 ml | B.45 ml. | C.30 mL | D.15mL |
Na2O2、CaC2都能与水反应,且反应中都有气体放出。下列说法正确的是
| A.都属于氧化还原反应 | B.生成的气体均为氧化产物 |
| C.反应物水均作氧化剂 | D.反应均放热 |
给汽车安装尾气净化装置,汽车尾气通过净化装置(内有钯等过渡金属元素做催化剂)后,其中的有害气体CO、NO转化为无害气体N2、CO2则( )
| | A. | NO作为还原剂 | B. | CO作为还原剂 | C. | N2作为还原剂 | D. | CO2作为氧化剂 |
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金——氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出。其反应原理为
①4Au+8NaCN+O2+2H2O 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。
以下有关氰化法提炼金的说法中正确的是
| A.Na[Au(CN)2]不溶于水 |
| B.化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C.金元素在地壳中能以化合态的形式存在 |
| D.在提炼过程中含金元素的物质始终作氧化剂 |
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50mg,则
| A.被氧化的砒霜为1.98mg |
| B.分解产生的氢气为0.672ml |
| C.和砒霜反应的锌为3.90mg |
| D.转移的电子总数为6×10―5NA |
下列试剂不会因为空气中的氧气而变质的是
| A.过氧化钠 | B.氢硫酸 | C.硫酸亚铁 | D.苯酚 |
下表中对应关系正确的是
| A | CH3CH3+Cl2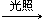 CH3CH2Cl+HCl CH3CH2Cl+HClCH2=CH2+HCl  CH3CH2Cl CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br?=2Cl?+Br2 Zn+Cu2+=Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O+4NaOH+O2↑ Cl2+H2O="HCl+HClO" | 均为水作还原剂的氧化还原反应 |
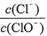 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是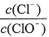 =11,则溶液中
=11,则溶液中 =
=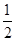
 amol
amol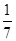 amol
amol