某澄清透明溶液中只可能含有:①A13+;②Mg2+;③Fe3+;④Cu2+;⑤H+;⑥ ;⑦
;⑦ 中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是
中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是
| A.②⑤⑦ | B.②⑤⑥ | C.③⑤⑦ | D.①④⑤ |
下列各组微粒在指定环境中一定可大量共存的是
A.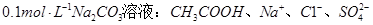 |
B.常温下,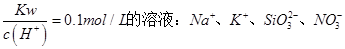 |
C.投入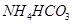 固体能产生气体的溶液: 固体能产生气体的溶液: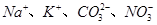 |
D.pH=1的溶液中: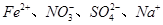 |
下列反应的离子方程式正确的是
A.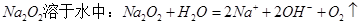 |
B.用FeC13溶液腐蚀电路板: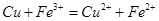 |
C.向 溶液中通入过量 溶液中通入过量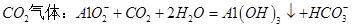 |
D.用食醋除去水瓶中的水垢: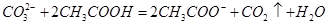 |
下列离子组在强酸性溶液中能大量共存、且溶液为无色透明的是
| A.NH4+、Al3+、SO42-、NO3- | B.Ag+、Na+、[Al(OH)4]-、Cl- |
| C.K+、NH4+、MnO4-、SO42- | D.K+、Na+、SO42-、HCO3- |
下列相关反应的离子方程式书写正确的是
| A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| B.钠与硫酸铜溶液反应:2Na+Cu2+==Cu+2Na+ |
| C.向硫酸铝溶液中加入过量氨水:Al3+ + 3OH-=Al(OH)3↓ |
| D.将铜片放入足量稀硝酸中:3Cu + 8H++ 2NO3- = 3Cu2+ + 2NO↑+ 4H2O |
某由离子化合物组成的混合物只可能含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、Cl-、CO32-、SO42-。为确定其组成,准确称取14.82g混合物溶于水得300 mL澄清溶液,分成三等份分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液并加热,经碱石灰干燥后收集到标况下气体1.12L
(3)第三份加足量BaCl2溶液,沉淀经洗涤、干燥后称重为6.27g,再向沉淀中加足量盐酸,经过滤、洗涤、干燥后称重为2.33 g
根据上述实验,以下推测不正确的是
| A.溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L |
| B.该混合物中不含Ba2+、Mg2+ |
| C.一定存在NH4+、 K+,无法确定Cl-是否存在 |
| D.实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响 |
下列离子方程式书写正确的是
| A.用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+= Cu2++2H2O |
B.实验室制氯气:MnO2+4HCl(浓) 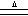 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| C.用FeS除去工业废水中的Hg2+:Hg2++S2-=HgS↓ |
| D.向次氯酸钠溶液中通入少量二氧化硫:ClO-+ SO2 + H2O = Cl-+SO42- + 2H+ |
已知:Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反,I2的氧化性比S强。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
| A.Fe2S3和 Al(OH)3 | B.Fe(OH)3和Al(OH)3 |
| C.FeS、Al(OH)3和S | D.Al2S3、FeS和S |
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL1mol·L-1的HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )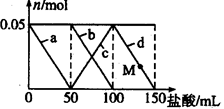
A.b曲线表示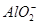 的减少,d曲线表示氢氧化铝的溶解 的减少,d曲线表示氢氧化铝的溶解 |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时Al(OH)3的质量小于3.9g |
D.原混合溶液中的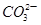 与 与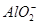 的物质的量之 的物质的量之 |
物质之间相互反应时,加入的量不同往往反应不尽相同,在给定条件下反应,下列叙述 正确的是( )
A.NaHCO3与石灰水反应,当n(NaHCO3):n[Ca(OH)2]=1︰1时,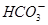 完全转化为CaCO3 完全转化为CaCO3 |
| B.CO2通入石灰水中,当n(CO2)︰n[Ca(OH)2]=1︰1时,能得到澄清溶液 |
C.AlCl3溶液与烧碱溶液反应,当n(OH-)︰n(Al3+)=1︰1时,铝元素以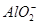 形式存在 形式存在 |
| D.Fe与稀硝酸反应,当n(Fe)︰n(HNO3)=1︰1时,溶液中铁元素只以Fe3+形式存在 |