下列离子方程式正确的是( )
| A.足量的CO2通入饱和碳酸钠溶液中: CO2+CO32-+H2O→2HCO3- |
B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O 4Fe3++4OH- 4Fe3++4OH- |
| C.次氯酸钙溶液中通入足量二氧化硫:Ca2++ClO-+SO2+H2O→CaSO4↓+Cl-+2H+ |
| D.碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO3-+2Ca2++4OH— ®2CaCO3↓+ Mg(OH)2↓+ 2H2O |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液中肯定不存在的离子组是( )
| A.Al3+、Mg2+、SO32- | B.Mg2+、CO32-、I- |
| C.Al3+、SO32-、I- | D.Al3+、Br-、SO32- |
某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ。为确认该溶液组成进行如下实验:①取20.0 mL该溶液,加入25.0 mL 4.00 mol·L-1NaOH溶液,有白色沉淀、无剌激气味气体。过滤、洗涤、干燥,得沉淀1.16 g。再将滤液稀释至100 mL,测得滤液中c(OHˉ)为0.20 mol·L-1;②另取20.0 mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48 g。由此可得出关于原溶液组成的正确结论是
| A.一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ |
| B.一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ |
| C.c (Clˉ) 为 4.00 mol·L-1,c (Al3+) 为1.00 mol·L-1 |
| D.c (Mg2+) 为 1.00 mol·L-1,c(Na+ ) 为 0.50 mol·L-1 |
下列离子方程式书写正确的是
| A.铁溶于盐酸中 2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O |
| C.二氧化硫被烧碱溶液吸收 SO2 +2OHˉ= SO32ˉ + H2O |
| D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O |
某溶液中存在大量的OHˉ、Clˉ、CO32ˉ,该溶液中还可能大量存在的是
| A.NH4+ | B.Ba2+ | C.Fe3+ | D.SO42ˉ |
水溶液中能大量共存的一组离子是:
| A.K+、Al3+、NO3-、CO32- | B.H+、Na+、Fe2+、NO3- |
| C.Na+、Ba2+、Cl-、NO3- | D.K+、NH4+、SO42-、OH- |
下列各组离子在通入SO2前后均能大量共存的是
| A.Ba2+、K+、Br-、Cl- | B.Na+、Cu2+、OH-、SiO32- |
| C.NH4+、Al3+、Br-、AlO2- | D.Li+、H+、NO3-、SO42- |
常温,下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1的溶液中: I-、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)="0.1" mol·L-1的溶液中:K+、ClO-、SO42-、SCN- |
下列离子方程式书写正确的是( )
A.碳酸钠溶液滴入酚酞变红: CO32- + 2H2O 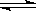 H2CO3 + 2OH- H2CO3 + 2OH- |
| B.铜溶解于氯化铁溶液中:2Fe3++3Cu=2Fe+3Cu2+ |
| C.氯化铝溶液与过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.FeSO4溶液中滴入稀硝酸:3Fe2+ + 4H+ + NO3- = 3Fe3+ + 2H2O + NO↑ |
下列分子或离子在指定的分散系中能大量共存的一组是
| A.碱性溶液中:ClO-、Cl-、K+、Na+ |
| B.常温常压下气体:O2、N2、Cl2、NH3 |
| C.含有AlO2-的溶液:NO3-、HCO3-、Na+、K+ |
| D.氢氧化铁胶体: H+、K+、S2-、Br- |