下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+ Fe3++3H2O Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HC +H2O +H2O H3O++C H3O++C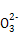 |
C.稀硝酸中加入足量的铁屑:3Fe+8H++2N  3Fe2++2NO↑+4H2O 3Fe2++2NO↑+4H2O |
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:N +Al3++2S +Al3++2S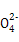 +2Ba2++5OH- +2Ba2++5OH- Al Al +2BaSO4↓+NH3·H2O+2H2O +2BaSO4↓+NH3·H2O+2H2O |
下表中有关离子方程式的评价合理的是( )
| 选项 | 化学反应及离子方程式 | 评价 |
| A | AlCl3溶液中加入过量氨水: Al3++3NH3·H2O  Al(OH)3↓+3N  | 错误,铝元素的产物应该是Al 或[Al(OH)4]- |
| B | 过量氯气通入溴化亚铁溶液中: 3Cl2+2Fe2++4Br-  6Cl-+2Fe3++2Br2 6Cl-+2Fe3++2Br2 | 正确 |
| C | 用氨水吸收过量二氧化硫: 2NH3·H2O+SO2  2N  +S +S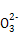 十H2O 十H2O | 正确 |
| D | 氯化铵溶于水: N  +2H2O +2H2O H3O++NH3·H2O H3O++NH3·H2O | 错误,氯化铵溶解于水是物理变化,不能写离子方程式 |
化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是( )
A.用食醋除去水壶内的水垢:CaCO3+2H+ Ca2++CO2↑+H2O Ca2++CO2↑+H2O |
B.纯碱溶液呈碱性的原因是:C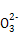 +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
C.钢铁发生吸氧腐蚀的正极反应式: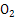 +4e-+2H2O +4e-+2H2O 4OH- 4OH- |
D.表示氢气燃烧热的热化学方程式为2H2(g)+O2(g) 2H2O(l) ΔH="-571.6" kJ· mol-1 2H2O(l) ΔH="-571.6" kJ· mol-1 |
下表对某些反应方程式的评价合理的是( )
| 编号 | 实验 | 离子方程式或电极反应式 | 评价 |
| A | 次氯酸钙溶液中通入足量SO2 | Ca2++ClO-+SO2+H2O CaSO4↓+Cl-+2H+ CaSO4↓+Cl-+2H+ | 正确 |
| B | Ba(OH)2溶液中加入过量Al2(SO4)3溶液 | 3Ba2++6OH-+2Al3++3S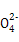  3BaSO4↓+2Al(OH)3↓ 3BaSO4↓+2Al(OH)3↓ | 正确 |
| C | 醋酸铵溶于水 | CH3COO-+N  CH3COOH+NH3·H2O CH3COOH+NH3·H2O | 错误,阴阳离子水解相互促进,应该用“ ”号 ”号 |
| D | 用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 | 阴极:Cu2++2e- Cu Cu阳极:4OH--4e-  2H2O+O2↑ 2H2O+O2↑ | 错误,只因为两极得失电子没配平 |
能正确表示下列反应的离子方程式的是( )
A.新制的氧化铝溶于氢氧化钠溶液:Al2O3+2OH- 2Al 2Al +H2O +H2O |
B.冷的氢氧化钠溶液中通入氯气:Cl2+OH- Cl-+HClO Cl-+HClO |
C.用KIO3氧化酸性溶液中的KI:5I-+I +3H2O +3H2O 3I2+6OH- 3I2+6OH- |
D.硫酸铝溶液中加入过量氨水:Al3++3OH- Al(OH)3↓ Al(OH)3↓ |
将铁铝矾[Al2Fe(SO4)4·xH2O]溶于水中,得到浅绿色溶液,有关该溶液的叙述正确的是( )
| A.铁铝矾有净水作用,其水溶液显中性 |
B.该溶液中:2c(Al3+)+c(Fe2+)+c(H+)=4c(S )+c(OH-) )+c(OH-) |
| C.在空气中,该溶液蒸干并灼烧,最后所得的残留固体为Al2O3、Fe2O3 |
D.向该溶液中加入Ba(OH)2溶液,当S 完全沉淀时,Al3+、Fe2+恰好被完全沉淀 完全沉淀时,Al3+、Fe2+恰好被完全沉淀 |
下列有关方程式书写正确的是( )
A.NaHCO3的电离:NaHCO3 Na++H++C Na++H++C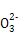 |
B.HS-的水解:HS-+H2O H3O++S2- H3O++S2- |
C.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e- 4OH- 4OH- |
D.用饱和Na2CO3溶液处理重晶石:BaSO4+C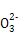  BaCO3+S BaCO3+S |
向100 mL 0.1 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )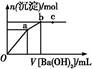
| A.a点时溶液中所含主要溶质为(NH4)2SO4 |
B.a→b段发生反应的离子方程式是:S +Ba2+ +Ba2+ BaSO4↓ BaSO4↓ |
| C.b点为最大沉淀量,对应的纵坐标值为0.02 |
| D.c点加入Ba(OH)2溶液的体积为200 Ml |
下列有关说法或方程式正确的是( )
A.用催化法处理汽车尾气中的CO和NO:CO+NO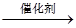 C+NO2 C+NO2 |
B.NO2与水的反应: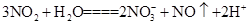 |
C.NH4HCO3溶于过量的NaOH溶液中: |
D.在1.0 mol·L-1的KNO3溶液中:H+、Fe2+、Cl-、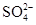 一定能大量共存 一定能大量共存 |
甲、乙、丙、丁四种易溶于水的物质,分别由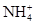 、Ba2+、Mg2+、H+、OH-、Cl-、
、Ba2+、Mg2+、H+、OH-、Cl-、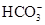 、
、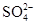 中的不同阳离子和阴离子各一种组成,已知:
中的不同阳离子和阴离子各一种组成,已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol/L乙溶液中c(H+)>0.1 mol/L;③向丙容器中滴入AgNO3溶液有不溶于稀硝酸的白色沉淀生成,下列结论不正确的是( )
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42+ |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |