设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.电解精炼粗铜时,每转移NA个电子,阳极溶解32g铜 |
| B.1L0.1mo1·L-1的氨水中含OH-离子数为0.lNA个 |
| C.常温常压下,a mo1O2与2a mo1NO混合,降温得到混合气体中氧原子数小于4aNA |
D.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA |
下列有关表示不正确的是
| A | B | C | D |
| 丁烷分子的球棍模型 | 质量数为A,中子数为a的X原子 | 邻羟基苯甲醛分子内氢键 | 放热反应的能量变化 |
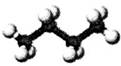 | A aX | 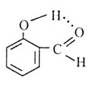 | 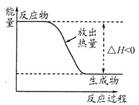 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.2.24L CH4气体中含有的电子数为NA |
| B.25℃时,1.0L PH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C.0.1NA个氯气份了溶于水形成1L溶液,所得溶液中c(C1-)=0.1mol·L-1 |
| D.1molCH3COONa和少量CH3COOH溶于水形成的中性溶液中,CH3COO-数目为NA |
将铁粉和铜粉的均匀混合物,平均分成四等分,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 mL | 200 mL | 300 mL | 400 mL |
| 剩余金属/g | 18.0 g | 9.6 g | 0 | 0 |
| NO体积/L | 2.24 L | 4.48 L | 6.72 L | V |
经化学定量分析,下列推断正确的是( )
A.①中溶解了5.6g Fe B.硝酸的浓度为4mol/L
C.②中溶解了9.6g Cu D.④中V=6.72 L
设NA表示阿伏加德罗常数的值。下列叙述不正确的是
| A.1 mol Na2O和Na2O2的混合物中含有的阴、阳离子总数是3NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| C.46 g有机物C2H6O中含有的H—O键的数目为NA |
| D.标准状况下,将0.1 mol Cl2通入足量NaOH溶液中,反应转移的电子数为0.1NA |
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
| A.1L0.1mol·L-1的氨水中含有的NH3分子数为0.1NA |
| B.标准状况下,2. 24L的CCl4中含有的C-Cl键数为0.4NA |
| C.常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA |
| D.标准状况下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.4NA |
下列化学用语表示正确的是 ( )
A.含18个中子的氯原子的核素符号: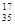 C1 C1 |
B.氟原子结构示意图: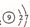 |
| C.1 -丙醇的结构简式:C3 H7OH |
D.CO( NH2)2的电子式: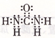 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.4.0 g重水(D2O)中所含中子数为1.6 NA |
| B.1 L 2 mol·L-1 K2S溶液中S2-和HS-的总数为2 NA |
| C.2.4g金刚石与石墨的混合物中所含碳原子数为0.2 NA |
| D.50 mL 18 mol·L-1浓硫酸与足量铜反应,转移的电子数为0.9 NA |
设NA为阿伏加德罗常数的值。下列说法一定正确的是
| A.25℃,pH=13的NaOH溶液中含有OH-为0.1 NA |
| B.1 L 0.1 mol·L-1 CuSO4溶液中含有Cu2+为0.1 NA |
| C.2.24LN2和NH3混合气体中原子间含有的共用电子对数目为0.3NA |
| D.2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA |
下列表述正确的是
| A.中子数为10的氧原子:18 10O |
B.Na2S的电子式: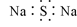 |
| C.聚氯乙烯的结构简式:CH2CHCl |
| D.Mg5(Si4O10)2(OH)2·4H2O的氧化物形式:5MgO·8SiO2·5H2O |