题目内容
下列表述正确的是
| A.中子数为10的氧原子:18 10O |
B.Na2S的电子式: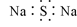 |
| C.聚氯乙烯的结构简式:CH2CHCl |
| D.Mg5(Si4O10)2(OH)2·4H2O的氧化物形式:5MgO·8SiO2·5H2O |
D
解析试题分析:A、中子数应该是18-10=8,错误;B、 Na2S是离子化合物,在电子式书写中要体现出阴阳离子的形式,错误;C、聚氯乙烯应该是结构式-[-CH2—CHCl-] n-,错误;
考点:考查基本的化学用语的书写和判断。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和○代表不同元素的原子。关于此反应说法错误的是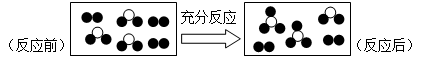
| A.一定属于可逆反应 | B.一定属于化合反应 |
| C.一定属于氧化还原反应 | D.一定属于放热反应 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温常压下,46gNO2含有3NA个原子 |
| B.7.8gNa2O2中含有的阴离子数目为0.2NA |
| C.室温时,1LpH=2的NH4Cl溶液中水电离出H+的数目为10-12NA |
| D.过氧化氢分解制得标准状况下1.12LO2,转移的电子数目为0.2NA |
下列有关化学用语使用正确的是 ( )
A.HClO的电子式: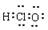 |
B.具有16个质子、16个中子和18个电子的微粒是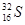 |
C.邻羟基苯甲酸的结构简式: |
D.乙烯的比例模型: |
设 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
A.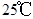 时,1g水中约含有6.02×1013个OH- 时,1g水中约含有6.02×1013个OH- |
B.在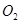 参与的反应中, 参与的反应中,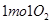 作氧化剂时得到的电子数一定是 作氧化剂时得到的电子数一定是 |
| C.1.8g重水(D2O)中含NA个质子和NA个中子 |
| D.标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA |
设NA表示阿伏加德罗常数的值。下列叙述不正确的是
| A.1 mol Na2O和Na2O2的混合物中含有的阴、阳离子总数是3NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| C.46 g有机物C2H6O中含有的H—O键的数目为NA |
| D.标准状况下,将0.1 mol Cl2通入足量NaOH溶液中,反应转移的电子数为0.1NA |
下列有关化学用语表述正确的是
A.原子结构示意图 可以表示35C1,也可以表示37C1 可以表示35C1,也可以表示37C1 |
| B.在标准状况下,纯水的pH=7 |
C.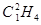 和 和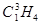 是同分异构体 是同分异构体 |
| D.葡萄糖的结构简式为C6H12O6 |
NA代表阿伏加德罗常数。下列有关叙述正确的是
| A.标准状况下,2.24LH2O含有的分子数等于0.1NA |
| B.20g重水(D2O)所含的电子数为10NA |
| C.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA |
| D.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
以NA表示阿伏加德罗常数,下列说法中正确的是
| A.在标准状况下,含4molHCl的浓盐酸与足量的MnO2反应可生成22.4L氯气 |
| B.0.1mol·L-1氯化钡溶液中Cl-数是0.2NA |
| C.18gD2O所含电子数目为10NA(相对原子质量:O-16) |
| D.4g氦气所含分子数为NA(相对原子质量:He-4) |