下列有关化学用语表示正确的是
A.S2-的结构示意图: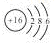 |
| B.常用于考古中文献年代确定的原子:14 6C |
C.H2CO3的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| D.4g H2在空气25℃.101kPa下燃烧,生成液态的水放出571.6kJ·mol-1的热量,则该反应的热化学方程式为:2H2(g)+O2(g)==2H2O(g);△H=-571.6kJ/mol |
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是
| A.分子总数为NA的SO2和CO2混合气体中含有的原子数为3NA |
| B.28 g乙烯和环丁烷(C4H8)的混合气体中含有的氢原子数为4NA |
| C.常温常压下,92 g的NO2和N2O4混合气体含有的氧原子数为4 NA |
D.标准状况下,22.4L氧气与足量铁粉充分反应,转移的电子数为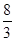 NA NA |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.往沸水中滴加0.1molFeCl3饱和溶液,制得的胶体中含0.1NA个Fe(OH)3胶体粒 |
| B.标准状况下,11.2L C2H6含3NA个C—H极性共价键 |
| C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,224mL水含有的电子数为0.1NA |
| B.1L 0.1mol/L硅酸钠溶液中含有0.1NA个SiO32- |
| C.足量的铁粉与lmolCl2在加热条件下充分反应,转移的电子数为3NA |
| D.标准状况下,11.2LCO2和SO2混合气体中含NA个氧原子 |
研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入5 mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法正确的是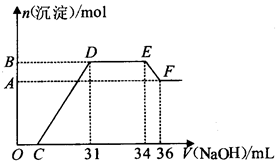
| A.溶液中结合OH-能力最强的离子是NH4+ |
| B.D点时溶液中存在:c(NH4+)+c(H+)=c(OH-)+c(NO3-) |
| C.合金中n(Fe) :n(Al)=1 :3 |
| D.C的值为7 |
NO、NO2、O2按照一定比例通入水中,能被完全吸收,无剩余气体,若NO、NO2、O2的气体体积分别为a、b、 c、则a:b:c可能为( )
| A.1:5:2 | B.2:5:1 | C.5:1:2 | D.5:2:1 |
下列有关说法不正确的是(NA表示阿伏加德罗常数)( )
| A.向硫酸酸化的KMnO4溶液中滴加BaCl2溶液,会产生白色沉淀和黄绿色气体 |
| B.室温下,42.0g乙烯和丁烯的混合气体中含有的碳原子数为3NA |
| C.CO32-离子的VSEPR模型为平面三角形 |
| D.19.5gNa2O2投入过量的水中,反应中转移的电子数为0.5NA |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol的2H35Cl含中子数为1.8NA |
| B.16g O3和O2混合物中氧原子数为NA |
| C.常温下,1L pH=l的溶液中H+的数目大于0.1NA |
| D.0.1 mol的H2O2中含有非极性键数为0.2NA |
两份质量相等的Na2O2和NaHCO3混合物,其中一份加入足量的盐酸充分反应后放出2.24L(标准状况)的气体;将这些气体通入另一份混合物中使其充分反应,气体体积变为2.016L(标准状况)。则原混合物中Na2O2和NaHCO3的物质的量之比为
| A.3:2 | B.2:1 | C.8:1 | D.2:9 |
如图,抽走玻璃片使氨气与氯化氢充分反应。下列有关描述合理的是(NA表示阿伏加德罗常数)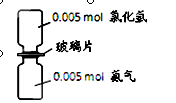
| A.反应前气体反应物的总体积为0.224 L |
| B.生成物的分子个数为0.005 NA |
| C.产物中的N-H键个数为0.02NA |
| D.加水溶解后所得溶液中NH4+数目为0.005 NA |