下列表述与化学用语正确的是
A.CO2的比例模型 |
B.氢化铵的电子式: 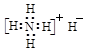 |
C.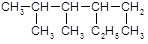 的名称:2,3-二甲基-4-乙基己烷 的名称:2,3-二甲基-4-乙基己烷 |
D.乙酸乙酯水解: |
有9.7 g Cu和Zn的合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2. 24 L。将溶液稀释为IL,测得溶液的pH=l,此时溶液中NO—3的浓度为
| A.0.3 mol/L | B.0.4 mol/L | C.0.5 mol/L | D.0.6 mol/L |
下列说法正确的是
| A.含有相同氧原子数的SO2和CO的质量相等 |
| B.等物质的量浓度的NaOH溶液与氨水中的c(OH—)相等 |
| C.等物质的量的甲基(—CH3)与羟基(—OH)所含电子数相等 |
| D.等温等压下,2 mol O2(g)和l mol SO2(g)的密度相等 |
下列对有关化学用语的理解错误的是
A.电子式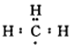 可以表示甲基,但是不可以表示CH+3 可以表示甲基,但是不可以表示CH+3 |
B.离子结构示意图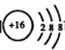 可以表示 可以表示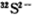 ,又可以表示34S2— ,又可以表示34S2— |
C.比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 |
| D.分子式C3H3O既可以表示1-丙醇,也可以表示2-丙醇 |
将2molNaHCO3和一定量的Na2O2固体混合,在加热的条件下使其反应,经测定无Na2O2剩余,则最后所得固体的物质的量(n)为
| A.1mol<n≤2mol | B.1mol<n≤4mol |
| C.2mol<n≤4mol | D.n>4mol |
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.(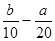 )mol/L )mol/L | B.(2b—a)mol/L | C.(l0b - 5a) mol/L | D.(5b一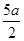 )mol/L )mol/L |
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
| A.OA段所发生反应的离子方程式: H++OH-=H2O;CO32-+H+=HCO3- |
| B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1。 |
| C.产生的CO2体积(标准状况下)为0.056 L |
| D.原NaOH溶液的物质的量浓度为0.5 mol·L-1 |
Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl―、OH―;且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
| A.2︰4︰1 | B.3︰2︰1 | C.2︰3︰1 | D.4︰2︰1 |
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1 mol,下列说法一定正确的是
| A.b=2 |
| B.容器中一定没有残余的CO2和水蒸气 |
| C.a:b≥1 |
| D.反应中转移的电子数一定为2NA |