某结晶水合物的化学式为R·nH2O,其相对分子质量为M。25 ℃时,a g该晶体能够溶于b g水中形成V mL溶液。下列关系中不正确的是
A.该溶液中溶质的质量分数为 |
B.该溶液的物质的量浓度为 |
C.该溶液中溶质与溶剂的质量比为 |
D.该溶液的密度为 |
某溶液中大量存在以下五种离子:NO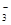 、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO
、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO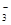 )︰n(SO42—)︰n(Fe3+)︰n(H
)︰n(SO42—)︰n(Fe3+)︰n(H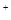 )︰n(M)=2︰3︰1︰3︰1,则M可能是下列中的
)︰n(M)=2︰3︰1︰3︰1,则M可能是下列中的
| A.Fe2+ | B.Cu2+ | C.Al3+ | D.Ba2+ |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,由N2与CO组成的28g混合气体中含有的原子数目为NA |
| B.常温下的新制氯水中,若含有Cl-的数目为NA,则其中含有ClO-的数目也为NA |
| C.常温常压下,将CO2通过足量Na2O2,若固体质量增加28g,参加反应的CO2分子数为NA |
| D.在反应2CuFeS2(二硫化亚铁铜)+O2=Cu2S+2FeS+SO2中,1mol硫被氧化时转移电子的数目为4NA |
下列变化一定属于化学变化的是
①风化 ②变色 ③燃烧 ④爆炸 ⑤白磷转变成红磷 ⑥工业制氧气 ⑦久置氯水变成无色 ⑧分馏 ⑨NO2气体冷却后颜色变浅 ⑩潮解
| A.①②③④⑦ | B.③④⑤⑦ | C.①③④⑦⑩ | D.①③⑤⑦⑨ |
有AlCl3和NaCl的混合溶液VL,将它均分成两份。一份滴加氨水,使Al3+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗a mol NH3·H2O、b mol AgNO3。据此得知原混合溶液中的c(Na+) (mol/L)为
| A.(2b-4a)/V | B.(b-a)/V | C.(2b-2a)/V | D.(b-2a)/V |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.0.1 mol Cl2完全溶于水,转移的电子数目为0.1NA |
| B.足量的硫单质与64g铜完全反应,转移电子数目为NA |
| C.1 mol Fe与足量的稀HNO3反应,转移2NA个电子 |
| D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1 |
下列有关“规定”正确的是
| A.PH小于7的雨水称为酸雨 |
| B.空气中直径大于2.5μm的颗粒物称为PM2.5 |
| C.分散质粒子直径介于1nm~100nm之间的分散系称为胶体 |
| D.标况下的气体摩尔体积为22.4L |
下列关于1 mol/L Na2SO4溶液的说法正确的是。
| A.溶液中含有1 mol Na2SO4 |
| B.1 mol Na2SO4溶于1 L蒸馏水中 |
| C.将322 g Na 2SO4·10H2O溶于少量水后再稀释到1000 mL |
| D.将322 g Na 2SO4·10H2O溶于少量水后再稀释到500 mL |
欲配制100 ml 1.0 mol/L Na2SO4溶液,正确的方法是
①将14.2 g Na2SO4 溶于100 ml水中
②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
| A.①② | B.②③ | C.①③ | D.①②③ |
当O2和O3的物质的量比之为3∶2时,它们具有相同的。
| A.原子数 | B.体积 | C.摩尔质量 | D.分子数 |