题目内容
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.0.1 mol Cl2完全溶于水,转移的电子数目为0.1NA |
| B.足量的硫单质与64g铜完全反应,转移电子数目为NA |
| C.1 mol Fe与足量的稀HNO3反应,转移2NA个电子 |
| D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1 |
B
解析试题分析:A在氯气和水的反应中每摩尔氯气参加反应,转移电子1mol。但0.1 mol Cl2完全溶于水时,发生反应的氯气的物质的量小于0.1mol,转移的电子数目小于0.1NA。错误。铜与硫反应生成硫化亚铜,每摩尔铜转移电子1摩尔。正确。CHNO3有强氧化性,Fe与足量的稀HNO3生成Fe(NO3)3. 1 mol Fe 3反应,转移3NA个电子.错误。D物质的量浓度是用指单位体积的溶液中所含溶质的物质的量来表示溶液组成的物理量,并非指溶剂的体积,错误。
考点:物质的量浓度的概念及可逆反应的特点、变价金属发生氧化还原反应时随氧化剂的量、浓度的变化而改变的情况的知识。

练习册系列答案
相关题目
在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(NO3-)为
| A.0.15 mol/L | B.0.20 mol/L |
| C.0.25 mol/L | D.0.40 mol/L |
将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g。另取等质量的合金溶于过量稀硝酸中,生成了6.72LNO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为
| A.22.1g | B.27.2g | C.30g | D.30.2g |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是 ( )
| A.28g乙烯所含共用电子对数目为4NA |
| B.0.5 mol 1, 3-丁二烯分子中含有C=C双键数为 NA |
| C.1 mol羟基所含的电子总数为10NA |
| D.标准状况下,11.2 L己烷所含分子数为0.5 NA |
下列溶液中,物质的量浓度最小的是
| A.1 L H2SO4溶液中含98 g H2SO4 |
| B.0.5 L含49 g H2SO4的溶液 |
| C.98 g H2SO4溶于水配成2 L溶液 |
| D.0.1 L含24.5 g H2SO4的溶液 |
某结晶水合物的化学式为R·nH2O,其相对分子质量为M。25 ℃时,a g该晶体能够溶于b g水中形成V mL溶液。下列关系中不正确的是
A.该溶液中溶质的质量分数为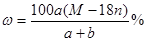 |
B.该溶液的物质的量浓度为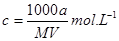 |
C.该溶液中溶质与溶剂的质量比为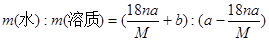 |
D.该溶液的密度为 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.标准状况下,22.4L CHCl3含有的分子数为NA |
| B.0.1mol/L的NH4NO3溶液中含有的氮原子数为0.2NA |
| C.1molFe2+与足量的H2O2溶液反应,转移2NA个电子 |
| D.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
下列化学用语使用正确的组合是
A.Mg2+结构示意图: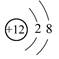 |
B.含18个中子的氯原子的核素符号: Cl Cl |
C.NH4Cl的电子式: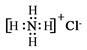 |
D.四氯化碳分子球棍模型:  |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A.标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA |
| B.56g的铁发生氧化还原反应,一定失去3NA个电子 |
| C.标准状况下,22.4L氟气中所含氟原子数为2NA |
D.0.1mol·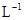 稀硫酸中含有 稀硫酸中含有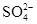 离子数为0.1NA 离子数为0.1NA |