NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A.在7.8gNa2O2晶体中阳离子与阴离子总数为0.3NA |
| B.在KIO3+6HI=KI+3I2+3H2O反应中,每生成3mol I2,则转移6NA个电子 |
| C.1mol Na2O2与H2O完全反应,转移的电子总数为NA |
| D.在1L0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8 mol·L-1,则c(K+)为
| A.0.15 mol·L-1 | B.0.2 mol·L-1 | C.0.3 mol·L-1 | D.0.4 mol·L-1 |
设NA为阿佛加德罗常数,下列叙述正确的( )
| A.标准状况下,NA个SO3分子所占的体积约为22.4 L |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.铁粉与一定量的浓硫酸反应,若产生11.2 L SO2和1 g H2,铁粉失去的电子数为2NA |
| D.50 mL 12 mol?L-1浓盐酸与足量二氧化锰反应,转移电子数为0.3 NA |
正确掌握化学用语和化学基本概念是学好化学的基础,下列有关表述中正确的一项是( )
| A.蔗糖与醋酸的最简式相同 |
| B.16O与18O互为同位素,H216O、D216O、H218O、D218O互为同素异形体 |
C.SiH4、CH4、 粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子 粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子 |
D.Ca2+的结构示意图为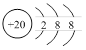 ;NH4Cl的电子式为 ;NH4Cl的电子式为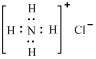 |
下列说法正确的是
| A.0.5mol SO2和11.2LCO2所含的分子数目一定相等 |
| B.25℃和100℃时,水的pH相等 |
| C.中和等体积、等物质的量浓度的NaOH和氨水所消耗的n(H2SO4)相等 |
D.2SO2(g)+O2(g) 2SO3(g) 和4SO2(g)+2O2(g) 2SO3(g) 和4SO2(g)+2O2(g)  4SO3(g)的△H相等 4SO3(g)的△H相等 |
NA为阿伏加德罗常数,下列各项叙述中,正确的有
①0.2 mol H2O2完全分解转移的电子数为0.4NA
②25 ℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA
③0.1 mol FeCl3滴入沸水形成的胶体粒子的数目为0.1 NA
④1 mol N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
| A.①②③ | B.①②④ | C.①②③④ | D.②④ |
NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.将28 g Fe投人到1 Ll mol/L的硫酸中,可得到11.2 LH2 |
| B.常温常压下,64 gSO2气体含有的原子数目为3 NA |
| C.25℃时pH =13的NaOH溶液中含有OH一的数目为0. 1 NA |
| D.1 mo1N a被完全氧化生成Na2O2,失去2 NA个电子 |
将一定量的Fe、Fe2O3、CuO的混合物放入体积为l00mL、浓度为2.2mol·L-1的H2SO4溶液中,充分反应后,生成气体 896mL(标况),得到不溶固体1.28 g,过滤后,滤液中的金属离子只有Fe2+(假设滤液体积仍为 100mL)。向滤液中滴加 2mol·L-1的 NaOH溶液至40mL时开始出现沉淀。则未滴加 NaOH溶液前滤液中 FeSO4的物质的量浓度为
| A.2 mol·L-1 | B.l.8 mol·L-1 | C.1.9 mol·L-1 | D.无法计算 |
两种金属混合物19.6克,投入到一定量的盐酸中,反应完全后得到11.2L(标准状况)的氢气,此金属混合物不可能是
| A.Mg和Al | B.Al和Fe | C.Mg和Cu | D.Fe和Zn |