实验室里需用480 mL 0.1 mol/L的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作正确的是( )
| A.称取7.68g硫酸铜,加入500mL水 |
| B.称取12.0g胆矾配成500mL溶液 |
| C.称取8.0g硫酸铜,加入500mL水 |
| D.称取12.5g胆矾配成500mL溶液 |
在V mL Al2(SO4)3溶液中含有Al3+m g,取V/4 mL该溶液用水稀释至4V mL,则SO42-物质的量浓度为
A.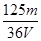 mol/L mol/L | B.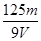 mol/L mol/L | C. mol/L mol/L | D.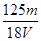 mol/L mol/L |
下列说法不正确的是
| A.在一定条件下,催化分解80g SO3,混合气体中氧原子数为3×6.02×1023 |
| B.一定条件下,铁与水蒸气反应生成8.96L H2时(已折合成标况),转移的电子数为0.8×6.02×1023 |
| C.100mL 1mol/L AlCl3与3mol/L NaCl的混合溶液中,Cl— 的个数为0.6×6.02×1023 |
| D.含有非极性键的数目为6.02×1023的Na2O2与水充分反应,标况下产生O2 22.4L |
若NA为阿伏加德罗常数的值,下列说法正确的是
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| D.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0. 2NA之间 |
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为ω,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( )
| A.ω=35a/(22.4Vρ) |
| B.c =a/(22.4V)mol/L |
| C.上述氨水中再加入等体积等浓度的稀盐酸后溶液恰好呈中性 |
| D.上述氨水中再加入V mL水后,所得溶液的质量分数小于0.5ω |
已知2Al+2NaOH+2H2O→2NaAlO2+3H2。对于该反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
| A.每生成0.6 mol H2,被还原的水分子数目为1.2NA |
| B.有2.7 g Al参加反应时,转移的电子数目为0.3NA |
| C.有6.72 L H2生成时,反应中转移的电子数目为0.6NA |
| D.溶液中每增加0.1mol AlO2-,Na+的数目就增加0.1NA |
把200mL NH4HCO3和Na2CO3 的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
| A.(l0b - 5a))mol/L | B.(2b-a)mol/L |
C.( )mol/L )mol/L | D.(5b-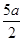 )mol/L )mol/L |
对于同温同压条件下的气体12C18O与14N2,判断正确的是
| A.体积相等时密度相等 | B.原子数相等时中子数相等 |
| C.体积相等时电子数相等 | D.质量相等时质子数相等 |
Al63Cu24Fe13是自然界中的一种天然准晶体,将相同质量的此准晶体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为
| A.n(盐酸)<n(稀硝酸)<n(烧碱) | B.n(烧碱)<n(盐酸)<n(稀硝酸) |
| C.n(烧碱)<n(稀硝酸)<n(盐酸) | D.n(稀硝酸)<n(烧碱)<n(盐酸) |
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子。则该硫酸盐的物质的量浓度为(NA表示阿佛加德罗常数的值)
| A.1mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.2 mol·L-1 |