题目内容
把200mL NH4HCO3和Na2CO3 的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
| A.(l0b - 5a))mol/L | B.(2b-a)mol/L |
C.( )mol/L )mol/L | D.(5b-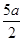 )mol/L )mol/L |
A
解析试题分析: NH4HCO3和amol NaOH恰好完全反应,则 NH4HCO3的物质的理为0.5amol,取另一份加入含bmol HCl的盐酸恰好反应完全,由 NH4HCO3反应掉的盐酸为0.5amol,则由Na2CO3 反应掉的盐酸为bmol-0.5amol,Na2CO3 的物质的量为(bmol-0.5amol)*0.5,则c(Na+)=(bmol-0.5amol)/0.1=(l0b - 5a))mol/L 。
考点:本题考查了物质的量浓度的计算。

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
用NA表示阿佛加德罗常数,下列叙述中正确的是
| A.常温常压下,22.4 L的氧气含氧原子数为2NA |
| B.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA |
| C.常温下,23g NO2含有NA个氧原子 |
| D.足量铜与1L 18mol·L-1浓硫酸反应可以得到SO2的分子总数为9NA |
标准状况下,均含有NA个电子的H2O和NH3,具有相同的
| A.质量 | B.物质的量 | C.体积 | D.氢原子数 |
有关四氯化碳的化学用语正确的是
A.结构简式: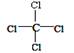 | B.电子式: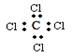 |
| C.结构简式:CCl4 | D.比例模型:  |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
| A.若M(甲)>M(乙),则气体体积:甲<乙 |
| B.若M(甲)<M(乙),则气体的压强:甲>乙 |
| C.若M(甲)>M(乙),则气体的摩尔体积:甲<乙 |
| D.若M(甲)<M(乙),则的分子数:甲<乙 |
在V mL Al2(SO4)3溶液中含有Al3+m g,取V/4 mL该溶液用水稀释至4V mL,则SO42-物质的量浓度为
A.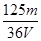 mol/L mol/L | B.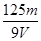 mol/L mol/L | C. mol/L mol/L | D.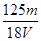 mol/L mol/L |
设NA为阿佛加德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有4NA个电子 |
| B.1L1mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| C.标准状况下,22.4L盐酸含有NA个HCl分子 |
| D.1molNa被完全氧化生成Na2O2,失去2NA个电子 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3 NA |
| B.25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2 NA |
| C.常温常压下,4. 4gCO2和N2O混合物中所含有的原子数为0.3 NA |
| D.标准状况下,2. 24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA。 |
下列说法中正确的是( )
| A.标准状况下,22.4L水中所含的分子数约为6.02×1023个 |
| B.1 mol Cl2参加反应转移电子数一定为2 NA |
C.标准状况下,aL氧气和氮气的混合物含有的分子数约为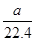 ×6.02×1023个 ×6.02×1023个 |
| D.从1 L 0.5 mol/LNaCl溶液中取出100 mL,,剩余溶液中NaCl物质的量浓度为0.45mol/L |