设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温下,23 g NO2含有NA个氧原子 |
| B.1 L 0.1 mol·L-1的氨水含有0.1NA个OH- |
| C.常温常压下,22.4 L CCl4含有NA个CCl4分子 |
| D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
| A.1 mol甲醇中含有C—H键的数目为4NA |
| B.25 ℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.标准状况下,2.24 L己烷含有分子的数目为0.1NA |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA |
下列叙述正确的是( )
| A.同温同压下,相同体积的物质,它们的物质的量必相等 |
| B.任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等 |
| C.1 L一氧化碳气体的质量一定比1 L氧气的质量小 |
| D.等体积、等物质的量浓度的强酸中所含的H+数目一定相等 |
下列关于物质的量、摩尔质量的叙述正确的是( )
| A.0.012 kg 12C中含有约6.02×1023个碳原子 |
| B.1 mol H2O中含有2 mol氢和1 mol氧 |
| C.氢氧化钠的摩尔质量是40 g |
| D.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
如图是某硫酸试剂瓶标签上的部分文字。据此,下列说法正确的是( )
| 硫酸 化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量的该硫酸反应生成2 g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2 mol/L
D.向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为w,其中含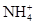 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w=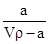 ×100% ×100% |
B.溶质的物质的量浓度c=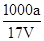 mol/L mol/L |
C.溶液中c(OH-)=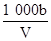 mol/L mol/L |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
某地酸雨经检验除含H+外[c(OH-)可以忽视]还有Na+、Cl-、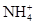 、
、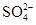 ,其浓度依次为:c(Na+)=2.3×10-5mol/L,c(Cl-)=3.5×10-5mol/L,
,其浓度依次为:c(Na+)=2.3×10-5mol/L,c(Cl-)=3.5×10-5mol/L,
c(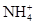 )=2.3×10-5mol/L,c(
)=2.3×10-5mol/L,c(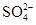 )=1.05×10-5mol/L。则该地酸雨的pH为( )
)=1.05×10-5mol/L。则该地酸雨的pH为( )
| A.3 | B.4 | C.5 | D.6 |
硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其同石灰乳混合可得“波尔多”溶液。实验室里需用480 mL 0.10 mol/L的硫酸铜溶液,则应选用的容量瓶规格和称取溶质的质量分别为( )
| A.480 mL容量瓶,称取7.68 g硫酸铜 |
| B.480 mL容量瓶,称取12.0 g胆矾 |
| C.500 mL容量瓶,称取8.00 g硫酸铜 |
| D.500 mL容量瓶,称取12.5 g胆矾 |
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 mol/L的碳酸钠溶液1 000 mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A.称取碳酸钠晶体100 g |
| B.定容时俯视刻度线 |
| C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 |
| D.定容后,将容量瓶振荡均匀,静置发现液面低于刻度线,于是又加入少量水至刻度线 |
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
| A.(b-a)/V mol·L-1 | B.(2b-a)/V mol·L-1 |
| C.2(b-a)/V mol·L-1 | D.2(2b-a)/V mol·L-1 |