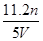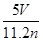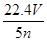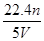用98%的浓硫酸(密度1.84g · mL-1)配制100mL 1mol·L-1的稀硫酸。现给出下列配制中可能用到的仪器:①100 mL量筒;②10 mL量筒;③50 mL烧杯;④托盘天平;⑤100 mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用仪器的先后顺序作出的下列排列中正确的是
| A.④③⑥⑦⑤⑥ | B.②⑥③⑦⑤⑥ | C.①③⑤⑦⑤⑥ | D.②③⑥⑦⑤⑥ |
设NA表示阿伏加德罗常数值,下列叙述正确的是
| A.常温常压下,56 g Fe与足量的盐酸完全反应转移的电子数为3NA |
| B.标准状态下,54g H2O中含有分子数为3NA个 |
| C.0.1 mol·L-1的硫酸铝溶液所含的SO42-数就是0.3NA |
| D.NA个He分子所具有的体积为22.4L? |
N0为阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol CO2中含有原子数N0 |
| B.1 L 1mol/L的硫酸钠溶液中,所含Na+数为N0 |
| C.标准状况下,11.2 L水所含分子数为0.5 N0 |
| D.在反应中,1 mol Fe和足量盐酸反应失去的电子数为2 N0 |
20mL 1mol ·L_1NaOH与1mol ·L_1的硫酸反应,溶液呈中性,则硫酸的体积为 ( )
| A.5 mL | B.l0 mL |
| C.20 mL | D.40 mL |
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A.1 mol甲基(—CH3)中含有电子数为7NA |
| B.25 ℃时,pH=7的NH4Cl和NH3·H2O的混合溶液中,OH-数为10-7NA |
| C.4.6 g乙醇中含有共价键数目为0.8NA |
| D.两份均为2.7 g的铝样品分别与100 mL浓度均为2 mol·L-1的盐酸和氢氧化钠溶液充分反应,转移电子数均为0.3NA |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.1 mol苯分子中含有碳碳双键数为3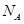 |
B.pH=13的氢氧化钠溶液中所含Na+为0.1 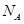 |
C.14g乙烯和丙烯的混合气体中所含原子总数为3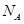 |
D.5.6g铁与足量的氯气反应失去电子数为0.2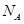 |
设阿伏加德罗常数的值为,则下列说法正确的是 ( )
A.标准状况下,22.4 L乙烯含有的共用电子对数为2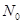 |
B.常温下,含有1 mol NaHSO4溶液中的阳离子数为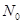 |
C.通常状况下,1 mol NO和0.5 molO2在密闭容器中混合,生成NO2分子数为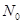 |
D.制取漂白粉时,标准状况下22.4 LCl2参加反应,转移电子数为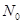 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是
| A.1 L1 mol/L氯化铜溶液中含有NA个Cu2+ |
| B.标准状况下,22.4 L O2参加任何化学反应转移的电子数都是4NA |
| C.1 mol Zn与足量稀HNO3反应,转移2NA个电子 |
| D.1 mol H3O+所含电子数为8NA |
设nA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4L O2与O3混合物含有3nA个氧原子 |
| B.0.1mol/L NH4Cl 溶液中含有NH4+ 数目为0.1nA |
| C.标准状况下,22.4LBr2与足量铁粉反应转移电子数目为2nA |
| D.17g H2O2含有 O-H键数目为nA |