题目内容
20mL 1mol ·L_1NaOH与1mol ·L_1的硫酸反应,溶液呈中性,则硫酸的体积为 ( )
| A.5 mL | B.l0 mL |
| C.20 mL | D.40 mL |
B
解析试题分析:根据题意知,20mL 1mol ·L_1NaOH与1mol ·L_1的硫酸反应,溶液呈中性,则二者恰好完全反应,氢氧化钠和硫酸的物质的量之比为2:1,根据公式n=cV判断,所需硫酸的体积为10mL,选B。
考点:考查物质的量浓度的计算。

练习册系列答案
相关题目
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.3mol NO2与水充分反应,转移nA个电子 |
| B.常温常压下,18g H2O含有3nA个原子 |
| C.1L 0.1 mol·L-1NaHCO3溶液中含有0.1nA个HCO3- |
| D.标准状况下,2.24L乙醇含有0.1nA个CH3CH2OH分子 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是
| A.1 L1 mol/L氯化铜溶液中含有NA个Cu2+ |
| B.标准状况下,22.4 L O2参加任何化学反应转移的电子数都是4NA |
| C.1 mol Zn与足量稀HNO3反应,转移2NA个电子 |
| D.1 mol H3O+所含电子数为8NA |
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A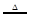 B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
| A.2d | B.10d | C.5d | D.0.8d |
同温同压下,等质量的O2和O3相比较,下列结论正确的是
| A.它们的分子数目之比是 1∶1 | B.它们的密度之比为 2∶3 |
| C.它们的体积之比是 1∶1 | D.它们的氧原子数目之比为 2∶3 |
下列说法正确的是( )。
| A.分子数不同的CO与N2的体积一定不等 |
| B.体积相同的CO与N2的质量一定相等 |
| C.质量相同、密度不同的CO与N2所含的原子数目一定相等 |
| D.质量不同、密度相同的CO与N2所含分子数可能相同 |
某溶液中大量存在以下浓度的五种离子:0.2 mol·L-1 Cl-、0.4 mol·L-1 SO42-、0.1 mol·L-1 Al3+、0.3 mol·L-1 H+、M,则M及其物质的量浓度可能为( )。
| A.Na+ 0.3 mol·L-1 | B.Zn2+ 0.2 mol·L-1 |
| C.CO32- 0.2 mol·L-1 | D.Ca2+ 0.1 mol·L-1 |
下列解释事实的方程式不准确的是 ( )。
| A.用浓盐酸检验氨:NH3+HCl=NH4Cl |
B.碳酸钠溶液显碱性:CO32—+H2O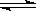 HCO3—+OH- HCO3—+OH- |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
| D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
设阿伏加德罗常数的数值为NA,则下列说法中正确的是( )。
| A.1.0 L 0.1 mol·L-1 Na2S溶液中含有的S2-离子数小于0.1NA |
| B.1 mol氯气与过量的Fe反应,转移电子的数目为3NA |
| C.2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
| D.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |