向10 g Fe2O3、SiO2和Al2O3的混合物中,加入100 mL x mol/L稀硫酸,过滤后,向滤液中加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。下列叙述错误的是( )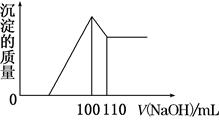
| A.混合物和稀硫酸反应时,稀硫酸过量 |
| B.可求出x的值 |
| C.可求出Al2O3的质量分数 |
| D.可求出Fe2O3的质量分数 |
设NA为阿伏加德罗常数的值,下列法说中正确的是( )
| A.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2 NA |
| B.标准状况下,2.24 L Cl2与足量的H2O反应,转移的电子总数为0.1 NA |
| C.标准状况下,22.4 L甲醇(CH3OH)中含有的氧原子数为1.0 NA |
| D.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移0.2 NA个电子 |
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示:
| 阳离子 | NH、Na+、Mg2+ |
| 阴离子 | OH-、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6 NA |
| B.常温常压下,46 g NO2与N2O4的混合气体中含有的分子总数为NA |
| C.25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA |
| D.一定量的钠与8g氧气作用,若两者均无剩余,转移NA个电子 |
NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,30 L pH=11的Na2CO3溶液中含有的OH-数为0.03NA |
| B.用含有0.1 mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C.25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D.100 mL 12 mol·L-l浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
下列说法正确的是
| A.1L 1mol?L-1的NH4Cl溶液中一定含有NA个NH4+ |
| B.常温常压下,22.4L乙烯中含极性共价键数为5 NA |
| C.6.8g熔融的KHSO4中含有0.05 NA个阳离子 |
| D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下反应可生成NA个H2O |
设NA代表阿伏加德罗常数的数值,则下列说法正确的是
| A.1.8 g D2O含有NA个中子 |
| B.用5 mL 3 mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
| C.在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4 L的CO2 |
| D.25℃时,7 g C2H4和C3H6的混合气体中,含有NA个C-H键 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,15 g甲基(-CH3)所含的电子数为7NA |
| B.水的摩尔质量就是NA个水分子的质量之和 |
| C.含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D.1 mo1Mg与足量O2或N2反应生成MgO或Mg3 N2均失去2NA个电子 |
把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.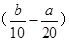 mol/L mol/L | B.(2b-a)mol/L | C.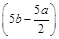 mol/L mol/L | D.(10b-5a)mol/L |
 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA