题目内容
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6 NA |
| B.常温常压下,46 g NO2与N2O4的混合气体中含有的分子总数为NA |
| C.25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA |
| D.一定量的钠与8g氧气作用,若两者均无剩余,转移NA个电子 |
A
解析试题分析:A、相同物质的量的乙烯和乙醇耗氧量相同,1mol消耗3mol氧气,正确;B、46 g NO2与N2O4的混合气体中含有的分子总数为0.5NA到NA之间,错误;C、溶液不知体积,无法计算离子物质量,错误;D、氧气与钠反应可以生成氧化钠(氧为-2价)也可以生成过氧化钠(氧为-1价),转移的电子数目分别为NA、0.5NA,错误。
考点:考查阿伏加德罗常数有关问题。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案将碳酸钠和碳酸氢钠的固体混合物Wg溶于水制成500mL溶液,钠离子的物质的量浓度为0.2mol?L-1,若将Wg该混合物用酒精灯加热至质量不再改变时,得到的固体物质的质量可能是
| A.5.3g | B.10.6g | C.4.2g | D.3.1g |
下列化学用语表达正确的是( )
A.Na2S的电子式: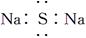 |
| B.铯137:137Cs |
C.O2-的结构示意图: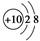 |
D.乙烯分子的球棍模型: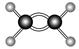 |
已知硫铁矿在沸腾炉中煅烧(4FeS2+11O2 8SO2+2Fe2O3),通入沸腾炉中的气体原料是过量的空气,其中N2的体积分数为0.80,O2的体积分数为0.20,则沸腾炉排出的气体中SO2的体积分数可能是( )
8SO2+2Fe2O3),通入沸腾炉中的气体原料是过量的空气,其中N2的体积分数为0.80,O2的体积分数为0.20,则沸腾炉排出的气体中SO2的体积分数可能是( )
| A.0.18 | B.0.12 | C.0.16 | D.0.20 |
把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.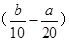 mol/L mol/L | B.(2b-a)mol/L | C.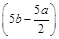 mol/L mol/L | D.(10b-5a)mol/L |
某混合气体X,可能由H2、CO、CO2和水蒸气中的一种或几种组成,现将混合气体通入灼热的CuO,完全反应后,固体CuO质量减少1.6 g;再将反应后的混合气体全部导入足量的澄清石灰水中,生成白色沉淀10 g。根据以上信息,分析下列有关X的组成推断正确的是( )
| A.X一定只由CO组成 |
| B.X一定只由H2和CO2组成 |
| C.X可能由0.1 g H2和4.4 g CO2组成 |
| D.X可能由0.1 g H2、1.4 g CO、2.2 g CO2组成 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.在1 L 0.1 mol/L硫化钠溶液中阴离子总数大于0.1NA |
| B.1 mol O2作氧化剂时转移电子数一定为4NA |
| C.标准状况下,22.4 L戊烷所含分子数为NA |
| D.在1 L 1.0 mol/L NaCl 溶液中含有NA个NaCl分子 |
下列说法正确的是( )
①有化学键破坏的变化一定属于化学变化 ②发生了颜色变化的一定是化学变化 ③电解质溶液导电一定发生了化学变化 ④用糯米、酒曲和水酿制成甜酒,一定是化学变化
| A.①③ | B.②③④ | C.③④ | D.全部 |
如图是NaCl、MgSO4的溶解度曲线。下列说法正确的是( )。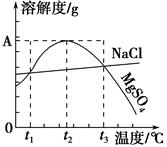
| A.只有在t1℃时,NaCl和MgSO4的溶解度才相等 |
| B.t1℃~t2℃,MgSO4的溶解度随温度升高而减小 |
| C.在t2℃时,MgSO4饱和溶液的溶质质量分数最大 |
| D.把MgSO4饱和溶液的温度从t3℃降至t2℃时,溶液的物质的量浓度减小 |