题目内容
NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,30 L pH=11的Na2CO3溶液中含有的OH-数为0.03NA |
| B.用含有0.1 mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C.25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D.100 mL 12 mol·L-l浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
A
解析试题分析:常温下,30 L pH=11的Na2CO3溶液中含有的OH-的物质的量为10-3×30L=0.03mol,所以OH-的个数为0.03NA,A选项正确;胶体粒子是氢氧化铁形成的集合体,微粒数一定小于0.1NA,故B错误;25℃时,pH=13的1LBa(OH)2溶液中含有的OH-的物质的量为10-1×1L=0.1mol,所以OH-的个数为0.1NA,C选项错误;依据化学方程式 MnO2+4HCl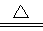 MnCl2+Cl2↑+H2O,100 mL×12 mol·L-l当1.2molHCl完全反应时可生成0.3NACl2,但随着反应的进行,盐酸的浓度逐渐降低,稀盐酸的还原性较弱,与二氧化锰不反应,则生成的氯气的物质的量小于0.3NA,D选项错误。
MnCl2+Cl2↑+H2O,100 mL×12 mol·L-l当1.2molHCl完全反应时可生成0.3NACl2,但随着反应的进行,盐酸的浓度逐渐降低,稀盐酸的还原性较弱,与二氧化锰不反应,则生成的氯气的物质的量小于0.3NA,D选项错误。
考点:考查了阿伏伽德罗常数。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
设NA代表阿伏加德罗常数,下列说法不正确的是
| A.4.6克钠与水反应时失去的电子数目为0.2NA |
| B.常温常压下2克氢气所含原子数目为NA |
| C.在标准状况下,22.4LNH3所含的分子数目为NA |
| D.1 L0.5mol?L-1Na2SO4溶液中所含有的Na+离子数目为NA |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.0.44 g C3H8中含有的共价键总数目为0.1NA |
| B.标准状况下,2.24 L三氯甲烷中含有碳氯共价键的数目为0.3NA |
| C.25 ℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| D.1 mol冰醋酸和1 mol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为NA |
36.5 g HCl溶解在1 L水中(水的密度近似为1 g/mL),所得溶液的密度为ρ g/mL,质量分数为w,物质的量浓度为c mol/L,NA表示阿伏加德罗常数的值,则下列叙述中正确的是( )
| A.所得溶液的物质的量浓度为1 mol/L |
| B.所得溶液中含有NA个HCl分子 |
| C.36.5 g HCl气体占有的体积为22.4 L |
| D.所得溶液的质量分数:w="36.5c/(1" 000ρ) |
向10 g Fe2O3、SiO2和Al2O3的混合物中,加入100 mL x mol/L稀硫酸,过滤后,向滤液中加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。下列叙述错误的是( )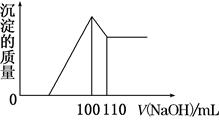
| A.混合物和稀硫酸反应时,稀硫酸过量 |
| B.可求出x的值 |
| C.可求出Al2O3的质量分数 |
| D.可求出Fe2O3的质量分数 |
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
| A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,18 g H2O中含有的原子总数为3NA |
| C.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA |
| D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
下列有关化学用语表示正确的是( )
| A.下图中的①是N2的电子式 |
| B.下图中的②是S2-的结构示意图 |
C.质子数为53,中子数为78的碘原子: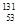 I I |
| D.下图③为CO2的结构式 |
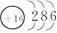 O—C—O
O—C—O① ② ③
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )。
| A.将NA个HCl分子溶于500 mL水中得到2.0 mol·L-1的盐酸 |
| B.在加热条件下,100 mL 18.4 mol·L-1的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92NA |
| C.密闭容器中,1 mol SO2与0.5 mol O2充分反应,转移的电子数小于2NA |
| D.用惰性电极电解AgNO3溶液,产生11.2 L O2时,转移2 mol电子 |